0 引言
种子播种前处理是蔬菜栽培的重要技术环节,可有效杀灭种子自身所带病菌,防止种子病害传播,降低生产成本,提高经济效益[5]。对西伯利亚、索邦等切花百合品种通过种子消毒处理,可有效防治百合刺足根螨、迟眼熏蚊幼虫、跳虫、线虫的发生[6-7];李诚[8]开展了室内种球消毒药剂筛选试验研究,证明多菌灵可以有效控制种传病害的发生流行。关于百合种子处理技术的应用研究集中于观赏百合,兰州百合是小宗山地旱作蔬菜,实际生产中农户基本不使用种子处理技术,鲜见此方面的研究报道。近年来,植物根际微生物群落组成对维持土壤健康所起的重要作用越来越被人们所重视。微生物在土壤生态系统中的功能通过维持土壤养分循环、生物控制土传病虫害、诱导植物抗病性等方式来实现,其丰度、多样性与植物种类、土壤类型及栽培技术密切相关[9]。功能益生菌对于植株生长、土壤养分及土壤健康的作用有较多报道,Sphingomonas已被大量报道为植物生长促进剂[10],并在病原菌的生物防治中发挥作用[11];Basidiomycota与土壤性质和香草枯萎病有关[12];Mortierella具有溶解土壤中磷的功能[13],可以促进土壤有机质和养分含量的提高。因此,研究根际土壤微生物对种子浸种处理的响应机制,对于种子处理技术提升及有益菌应用具有重要意义。
种子表面消毒可有效杀灭种子表面微生物,该技术已在观赏百合上成功应用[14-15]。多菌灵是高效、低毒的广谱性杀菌剂,可以有效防治作物的多种病害;阿维菌素是高效低毒生物农药,广泛应用于植物害虫防治;以生根粉及磷酸二氢钾浸种具有刺激种子萌发和促进壮苗壮根的作用,价格低,在农、林、园艺业中得到广泛应用。据此,本项目组于2018年,围绕种子消毒,配合使用发根激素及磷酸二氢钾,设计浸种剂配方,发现该浸种剂处理,可以有效促进兰州百合幼苗生长。2019年继续选择该配方研究,再次证明了其促进百合幼苗生长的作用效应,2021年田间测产结果表明,该配方显著提高了百合产量。兰州百合为无性繁殖植物,种球带根(1 cm)播种。浸种处理实现种子表面消毒的同时,对种球周围土壤及根际土壤在一定程度上产生了影响,形成了独特的土壤微生物环境,使得植物生理状态发生改变,从而引起根际微生物区系发生变化。因此,种球浸种处理与苗期根际微生物菌群可能存在一定的关联性。基于上述分析,本研究应用基因二代测序技术,对该配方浸种处理后的百合幼苗根际土壤微生物进行16S rRNA和ITS rRNA测序分析,研究其真菌与细菌群落结构的变化特点,以期寻找与百合幼苗生长相关的关键细菌与真菌微生物类群,为阐明种子表面消毒处理所引起的植物根际土壤微生物调节机制提供依据。
1 材料与方法
1.1 试验区简介及试验设计
试验地点位于甘肃省临洮县中铺镇蒋家山村(35°49′11″—35°49′13″N、103°53′12″—103°53′14″E,海拔2 330 m),属于典型的二阴山区,半湿润,无霜期较短,适宜种植兰州百合。试验地块前茬作物为兰州百合,收获后空闲一年用于本项研究。将微肥、生根粉及杀菌杀虫剂组合,为种子发芽提供营养,促进生根,同时实现种子表面消毒。
试验采用随机区组设计,设置SD(浸种处理)与CK(不浸种,直接播种)共2个处理,每个处理3次重复。磷酸二氢钾0.33 g·L-1+生根粉1.67 g·L-1+多菌灵0.33 g·L-1+阿维菌素0.20 g·L-1浸种,将百合种球(质量17±2 g,大小一致)用浸种剂浸泡4 h,晾干15 h后播种。播种时间为2019年4月18日。株距、行距、播种深度分别为20 cm、42 cm、10 cm,每小区6行,小区面积7.5 m×2 m。常规田间管理,旱作栽培,无灌溉。
1.2 土样的采集
土壤样品于百合苗期(2019年6月12日)采集。每小区随机选择5株植株,利用抖根法获得根际土壤。在靠近根部,用铲子铲除表层的土壤,采集深度为5—20 cm处的土壤;将植株根际周围的土壤抖落至自封袋中,用四分法保留1 kg左右土样,分成两份保存。取其中一份土壤样品过1 mm筛,保存在4 ℃冰箱用于微生物测定。
1.3 生长指标及产量的测定
百合于2019年4月18日播种,于播种30 d后测定发芽势,播种后36 d测定发芽率。发芽率(%)=播种36 d的发芽数/种子总数×100%;发芽势(%)=播种30 d的发芽数/种子总数×100%;在兰州百合苗期(2019年6月12日)、鳞茎膨大期(2019年7月28日)、枯萎期(2019年9月28日),每个处理随机选择5株,进行株高、茎粗、地上(地下)部干(鲜)重测定[16];用数显电子游标卡尺测定茎粗(植株根颈处的直径),用卷尺测定株高(植株根颈至生长点);将植株从根颈部位切断,用百分之一电子天平分别称量植株地上部、地下部重量,测定鲜重。干重测定时将称完鲜重的植株在105 ℃烘箱中杀青15 min后,于60 ℃下烘干至恒重,用百分之一电子天平称重。壮苗指数=(茎粗/株高+地下部分质量/地上部分质量)×全株重;根冠比=地下部分质量/地上部分质量。
种植当年(2019年9月28日)在各小区内随机选取20株测鳞茎质量。栽培3年之后,于2021年1月3日收获试验田百合,测定小区产量。
1.4 IlluminaMiseq高通量测序
DNA提取及PCR扩增在已发表的文章中有详细描述[17]。在PCR扩增的过程中,细菌16S rRNA基因的V3-V4高变区由正向引物338-F(5'-ACTCCTACGGGAGGCAGCAG-3')和反向引物806-R(5'-GGACTACHVGGGTWTCTAAT-3')产生,真菌扩增子由正向引物ITS1-F(5'-CTTGGTCATTTAGAGGAAGTAA-3')和反向引物ITS1-R(5'-TGCGTTCTTCATCGATGC-3')产生,在Allwegene Company(北京)的Miseq平台上进行深度测序。运行后,使用Illumina Analysis PipelineVersion2.6执行图像分析、碱基检出和错误估计。
1.5 数据分析方法
采用Microsoft Excel 2010软件进行原始数据处理及图表绘制,SPSS 22.0统计软件进行方差分析,利用Duncan's多重比较法进行差异显著性检测(P<0.05)。16S序列的分类学根据SILVA数据库[18]和Greengene数据库[19]比对进行,ITS1序列的分类根据UNITE数据库[20]比对进行。在OTU水平上,利用维恩图、Alpha多样性指数、Principal Components Analysis(PCA)分析处理间微生物群落的多样性;利用Linear Discriminant Analysis Effect Size (LEfSe)方法分析处理间产生显著差异的重要微生物类群。具体方法及所用软件详见本课题组已发表论文[17]。
1.6 登录号
本研究中获得的序列已提交至NCBI序列读取档案(SRA),编号为Bioproject ID PRJNA805390。
2 结果与分析
2.1 浸种处理对百合幼苗生长发育的影响
SD处理对百合植株部分生长发育指标产生显著影响(表1)。尽管SD处理对于发芽率及发芽势没有显著影响,但显著促进了百合植株的生长发育。壮苗指数是反映植株综合性生长的重要指标。根冠比可准确地反映植株同化产物的分配情况,合理的根冠比对促进作物增产具有重要作用。兰州百合苗期、鳞茎膨大期的壮苗指数(干)、根冠比(干)在处理间差异性显著,SD处理中鳞茎膨大期的壮苗指数(干)、根冠比(干),苗期的壮苗指数(干)、根冠比(干)较CK处理分别增加33.35%、66.38%,11.73%、60.48%;SD处理对于百合鳞茎的生长具有显著的促生效应,种球经过一个生长季节,SD处理的鳞茎质量比CK显著增加了5.49%。栽培3年之后收获的商品百合,经济产量比CK显著增加了6.61%。
表1 浸种(SD)处理对兰州百合植株综合生长指标及产量指标的显著性分析
Table 1
| 处理 | 发芽期 | 苗期 | 鳞茎膨大期 | 枯萎期 | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 发芽势 | 发芽率 | 壮苗指数 (鲜) | 壮苗指数(鲜) | 根冠比(干) | 壮苗指数 (干) | 壮苗指数 (鲜) | 根冠比(干) | 鳞茎质量 /g | 经济产量 /(kg·hm-2) | ||||
| CK | 0.46±0.11a | 0.74±0.07a | 15.62±0.39b | 77.53±1.61a | 1.79±0.03b | 30.49±2.63b | 171.55±20.60a | 2.10±0.17b | 27.05±0.78b | 5 336.11b | |||
| SD | 0.52±0.01a | 0.79±0.02a | 20.83±0.20a | 76.16±7.78a | 2.00±0.02a | 50.73±7.47a | 196.40±8.85a | 3.37±0.69a | 28.54±1.24a | 5 688.89a | |||
枯萎期由于地上部分凋萎,部分植株残体落入土壤中,因此,本生育时期仅测定了地下部分生长量,无壮苗指数与根冠比。鳞茎质量指种球浸种后生长一年后的质量,2019年9月28日通过对田间随机选取的20株百合的鳞茎质量测定获得。经济产量指鳞茎生长3年且质量在30 g以上,作为商品的鳞茎产量,2021年10月3日通过测定小区产量获得。不同小写字母表示差异显著,P<0.05。
2.2 浸种处理后对土壤微生物多样性质量及群落整体结构变化的影响
图1
图1
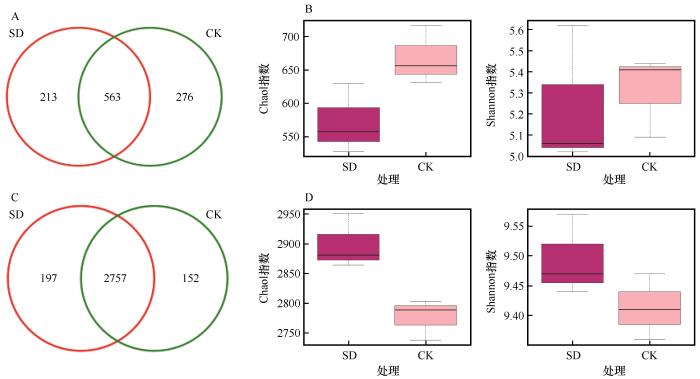
兰州百合种球浸种处理后根际土壤OTU分布及多样性分析:真菌Venn图(A),真菌Chaol、shannon指数图(B),细菌Venn图(C),细菌Chaol、Shannon指数图(D)
Fig.1
The distribution and diversity analysis of rhizosphere soil OTU after Lanzhou lily bulb seed soaking treatment: Fungus Venn diagram (A), fungus Chaol, Shannon index diagram (B), bacteria Venn diagram (C), bacteria Chaol, Shannon index diagram (D)
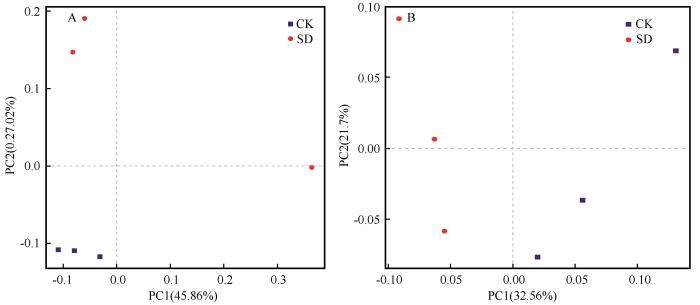
基于OTUs的真菌与细菌的PCA分析显示,SD与CK两个处理的各重复在处理间可以明显分开。真菌PCA分析显示,PC1和PC2共解释了72.88%的变异(图2)。细菌PCA分析表明,PC1和PC2共解释了54.26%的变异。
图2
图2
兰州百合种球浸种处理后根际土壤真菌的PCA(A)以及细菌的PCA(B)
Fig.2
The rhizosphere soil fungi PCA (A) and bacteria PCA (B) after Lanzhou lily bulb seed soaking treatment
2.3 根际土壤微生物群落结构
真菌相对丰度(Relative Abundance,RA)分析结果显示,在门水平上,优势类群为Ascomycota、Mortierellomycota
图3
图3
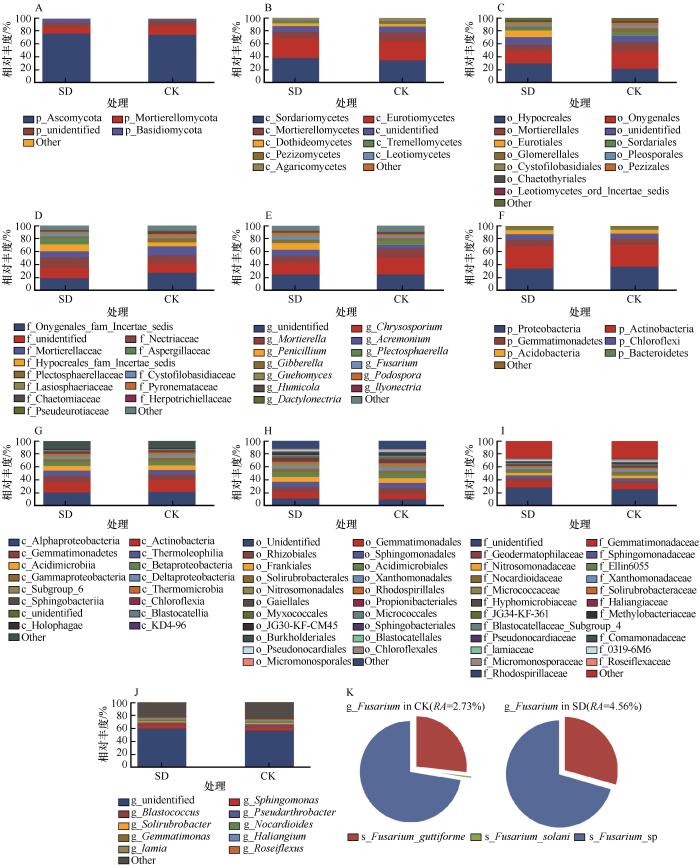
兰州百合种球浸种处理后根际土壤真菌(A—E)及细菌(F—J)各分类级别及镰刀菌属(K)的群落结构
Fig.3
The microorganism community structures of rhizosphere soil after soaking the seeds of Lanzhou lily bulb: fungal (A-E), bacterial phyla (F-J), and the genus Fusarium (K)
细菌门水平上的相对丰度结果显示,优势门为Proteobacteria、Actinobacteria、Gemmatimonadetes、Chloroflexi、Acidobacteria (平均RA>5%),总和分别占SD、CK细菌总数的93.54%、94.04%;SD、CK分别有0.29%、0.22%的序列不能鉴定(图3);优势纲为Alphaproteobacteria、Actinobacteria、Gemmatimonadetes、Thermoleophilia、Acidimicrobiia、Betaproteobacteria(平均RA>5%),总和分别占SD、CK细菌总数的67.77%、68.92%;优势目为Gemmatimonadales、Rhizobiales、Sphingomonadales、Frankiales、Acidimicrobiales、Solirubrobacterales(平均RA>5%),总和分别占SD、CK真菌总数的46.00%、44.28%;优势科为Gemmatimonadaceae、Geodermatophilaceae
2.4 不同处理优势微生物类群的LEfSe分析
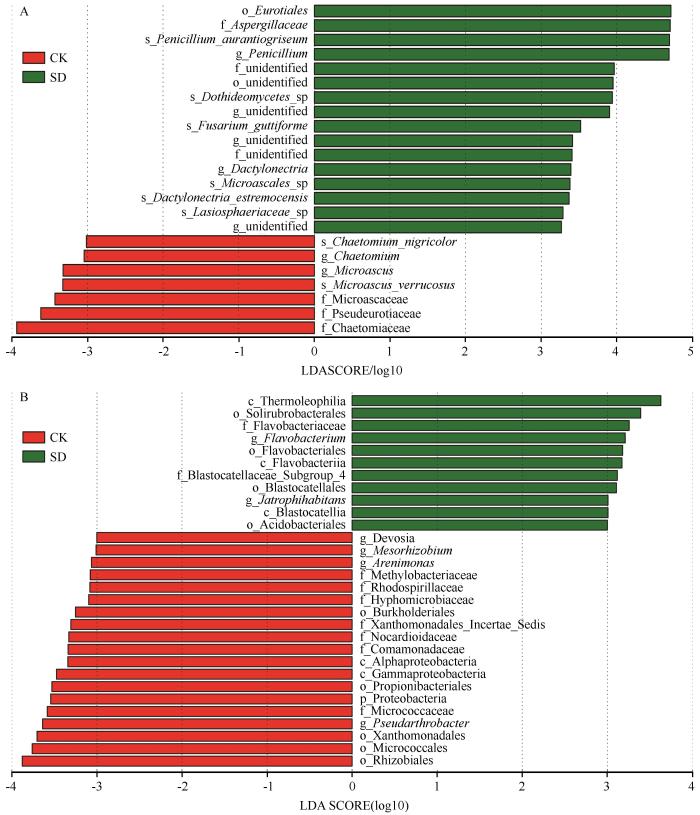
LEfSe分析展现了处理间不同层级丰度有显著性差异的优势物种。真菌群落LEfSe分析结果显示,在CK与SD之间,各优势门差异不显著。在属水平上,SD处理中隶属于Ascomycota门的成员属Penicillium RA显著增加;CK处理中,隶属于Ascomycota门的Microascus、Chaetomium属RA显著增加。但Ascomycota门含量在两处理间差异并不显著,在种水平上,SD处理中Penicillium aurantiogriseum、Dothideomycetes sp.、Fusarium guttiforme、Microascales sp.、Dactylonectria estremocensis、Lasiosphaeriaceae sp的RA显著增加;CK处理中Chaetomium nigricolor、Microascus verrucosus RA显著增加(图4)。
图4
图4
基于 LEfSe分析的兰州百合种球浸种处理后根际土壤真菌(A)及细菌(B)群落相对丰度的变化
Fig.4
LEfSe analysis showing the relative abundance of fungal (A) and bacterial (B) communities in the rhizosphere soil after soaking of Lanzhou lily bulbs
百合根际土壤细菌群落LEfSe分析结果显示,CK中的Proteobacteria门丰度显著大于SD处理。在种水平下,SD处理中,Bacteroidetes门下的Flavobacterium属和Actinobacteria门下的Jatrophihabitans属的RA显著增加。CK处理中,Proteobacteria门的成员属Devosia、Mesorhizobium、Arenimonas的RA显著增加,Actinobacteria门成员属Pseudarthrobacter的RA显著增加。在种水平上,未能检测到差异显著性物种存在(图4B)。
3 讨论
3.1 土壤微生物多样性
在自然界中,土壤生物多样性与土地生产力水平及其可持续性存在正相关关系[21]。土壤生物多样性对耕作制度、耕作方法及施肥等土壤管理措施的变化很敏感[22]。微生物多样性是土壤生物多样性的重要组成部分。本研究结果表明,SD处理对百合根际土壤微生物的Alpha多样性产生一定的影响,可引起土壤细菌丰度指数(Chao1)显著增加(图1),该变化可能是其提高土壤健康性的作用机制之一。SD处理引起土壤细菌丰度增加,其原因可能是SD处理后,植物根际形成了一个相对洁净的土壤微环境,有利于细菌的增殖;然而,SD处理对根际土壤真菌丰度没有显著影响,可能因为本研究使用的浸种剂配方含有多菌灵成分,该药剂主要对真菌起作用,由此导致真菌群落的恢复速度低于细菌群落。
3.2 与百合植株生长相关的特定土壤真菌群落
本研究结果还表明,Penicillium属是对兰州百合植株生长产生正效应的重要微生物类群。LEfSe分析结果显示,SD处理后Penicillium的RA显著增加,SD处理中Penicillium的RA为10.14%,而CK中Penicillium的RA为0.38%,前者是后者的26.68倍(图4)。Penicillium能够产生多种生物活性化合物,并作为真菌拮抗剂和植物生长促进剂[23-24];刘西莉等[25]研究表明,带有Penicillium等微生物的大豆种衣剂包衣处理具有种子消毒、提高出苗率、促进壮苗等多方面的综合效能。在本研究中,该属的一个种Penicillium aurantiogriseum在SD中丰度显著高于CK(图3)。P. aurantiogriseum具有溶解土壤中磷的功能[26],因此,Penicillium及其种P. aurantiogriseum对植株生长和正向调控作用,可能通过对病原菌的拮抗作用及对土壤的解磷作用来实现。
Microascus、Chaetomium为益生菌,具有潜在的生防能力及对植物的促生作用[27-28]。然而,本研究中,SD处理中Microascus、Chaetomium的RA显著降低(图4),可能因为本研究使用的SD浸种剂配方含有多菌灵成分,Microascus、Chaetomium可能对该杀菌剂较为敏感,导致其RA显著低于CK。本研究还检测到Dothideomycetes sp.,Microascales sp.,Lasiosphaeriaceae sp.在SD处理中显著增加。这3类真菌对于植物的促生作用已有文献零星报道,Dothideomycetes sp.对蓝莓和笃斯越橘的生物量、根长、分枝数及株高具有显著促进作用[29];Microascales sp.对荧光假单胞菌、枯草芽孢杆表现出抑菌活性,具有广谱抑菌效果[30],Lasiosphaeriaceae sp.与蓝盆花(Scabiosa tschiliensis Grunning)株高呈显著正相关[31]。由此推测,上述3个真菌类群有可能也对兰州百合植株生长产生促生作用,有必要对其分离培养,深入研究其功能作用。
Fusarium ssp.是可能引起作物发生土传病害的重要病原真菌。我们前期研究表明,Fusarium的积累在兰州百合连作障碍发生中起重要作用[17],在本研究中,Fusarium是优势属之一(TOP7,平均RA为3.64%,图3),但其丰度在处理间差异并不显著。在该属中,我们鉴定到了两个种——F. guttiforme和F. solani,其中F. guttiforme是优势种(平均RA=1.03%),与CK相比,在SD中显著增加,而F. solani丰度很低(平均RA=0.01%),其RA在处理间差异并不显著。该结果提示:与F. solani相比,消毒处理后所形成相对洁净的土壤环境,更加易于F. guttiforme定殖与增殖。F. solani是引起兰州百合枯萎病的病原真菌[3];F. guttiforme是菠萝枯萎病的重要病原菌[32],但该种是否为百合枯萎病的致病菌未见报道。另一方面,本研究中,Fusarium属中仅有1/3的序列鉴定到种水平(平均RA=1.04%),2/3和序列无法鉴定到种(平均RA=2.60%)。因此,本方法浸种处理是否对由于Fusarium ssp.引起的百合土传病害的防治产生直接作用,结论尚不明确,有必要进行深入研究。
3.3 与百合植株生长相关的特定土壤微细菌类群
Actinobacteria、Proteobacteria、Gemmatimonadetes、Chloroflexi、Acidobacteria是百合根际土壤中的优势细菌门(图3),该结果支持我们关于兰州百合根际土壤细菌优势群落的研究结果[33]。关于Proteobacteria,有文献报道该类细菌与烟草青枯病的发病率呈正相关[34]。我们前期对0—9年的兰州百合连作栽培土壤劣化过程研究发现,Proteobacteria及其包含的属Sphingomonas可以作为土壤健康性的标志,其丰度与土壤健康性呈正相关,随着连作年限的增加,Sphingomonas的耗竭是百合连作土壤退化的重要原因[33]。本研究中检测到Proteobacteria门与Sphingomonas属(TOP1,平均RA为4.22%),但是,与CK相比,SD处理中Proteobacteria的RA显著减少(图4),Sphingomonas属RA在SD与CK间差异不显著。该现象出现原因可能与SD处理后形成的特定的土壤环境条件有关。
在属水平上,SD处理中,益生细菌Flavobacterium,Jatrophihabitans丰度增加及有害细菌Devosia丰度降低,可能是浸种处理对兰州百合产生促生效应的重要机理。Flavobacterium属是潜在的植物生长促进根际细菌,具有较好的解磷能力,可以促进水稻的生长[35],还可以产生挥发性物质,对辣椒疫霉菌(Phytophthora capsici)具有显著的生防活性[36];高山生姜姜瘟病生物防治的研究表明,Jatrophihabitans属是有益菌放线菌,其丰度增加有利于土壤微生态朝健康方向发展[37];来自于苹果连作障碍的研究结果表明:Devosia属为有害微生物,其相对丰度与苹果连作病害发病率相关[38]。本研究还发现,在SD处理中,Mesorhizobium、Arenimonas和Pseudarthrobacter的RA显著降低。Mesorhizobium是具有生物肥料作用的植物根际促生菌菌株[39],Pseudarthrobacter有可能增加植物根际速效养分的含量[40]。出现该结果的原因可能是上述3类微生物对于土壤环境较为敏感,SD处理后造成的特定的根际土壤微环境不利于该类细菌的生长或群落的恢复(图4)。
兰州百合种球浸种处理与苗期根际微生物菌群变化存在关联性,种球表面消毒可引起百合苗期根际土壤微生物区系重建。兰州百合种球播种时带根,播种前需要将根稍修剪(修剪至1 cm左右,以方便农事操作)。因此,浸种处理实现种子表面消毒的同时,对种子及根系周围的土壤在一定程度上也起到了消毒作用,形成了相对洁净的土壤环境,使得根际微生物区系发生改变;另一方面,由于浸种处理改变了百合根系及幼苗的生理状态,诱导其根系分泌物发生改变,从而对根际微生物种群形成了新的选择压力,导致微生物群落结构发生变化[9,41];我们前期研究证明,兰州百合在不同的生理状态条件下,其根系分泌物不同[42]。据此推论,浸种处理引起百合根系形态以及根系分泌物发生改变,是微生物类群发生变化的另一基本原因。
4 结论
浸种处理有效促进了兰州百合植株的生长,改变了植物根际土壤真菌和细菌的群落结构,显著提高了土壤细菌丰度;在百合根际土壤中出现了一些与幼苗生长相关的特定的关键微生物类群。益生真菌属Penicillium及其种Penicillium aurantiogriseum,益生细菌属Flavobacterium,Jatrophihabitans在根际土壤中富集,有害细菌属Devosia减少,是浸种处理提高了土壤健康,对幼苗生长产生促进作用的根际土壤微生物区系调节机理。
参考文献
连作栽培对兰州百合(Lilium davidii var.unicolor)叶片PSⅡ光化学效率和抗氧化作用的影响
[J].
Plant species and soil type cooperatively shape the structure and function of microbial communities in the rhizosphere
[J].
Fine-needle aspiration diagnosis of GIST:a diagnostic dilemma
[J].
Protection of Arabidopsis thaliana against leaf-pathogenic Pseudomonas syringae by Sphingomonas Strains in a controlled model system
[J].
Different continuous cropping spans significantly affect microbial community membership and structure in a vanilla-grown soil as revealed by deep pyrosequencing
[J].
Soil fungal diversity loss and appearance of specific fungal pathogenic communities associated with the Consecutive Replant Problem (CRP) in Lily
[J].
The SILVA ribosomal RNA gene database project:improved data processing and web-based tools
[J].
Greengenes,a chimera-checked 16S rRNA gene database and workbench compatible with ARB
[J].
Gapped BLAST and PSI-BLAST:a new generation of protein database search programs
[J].
Modelling the effects of loss of soil biodiversity on ecosystem function
[J].
Soil arthropods in maintaining soil health:thrust areas for sugarcane production systems
[J].
Rhizo-sphere bacteria and fungi associated with plant growth in soils of three replanted apple orchards
[J].
Plant growth promotion and Penicillium citrinum
[J].
Effects of leaf scales of different pineapple cultivars on the epiphytic stage of Fusarium guttiforme
[J].
Bacterial communities as indicators of soil health under a continuous cropping system
[J].
Significant relationship between soil bacterial community structure and incidence of bacterial wilt disease under continuous cropping system
[J].
Flavobacterium pokkalii sp.nov.,a novel plant growth promoting native rhizobacteria isolated from pokkali rice grown in coastal saline affected agricultural regions of southern India,Kerala
[J].
The volatile-producing Flavobacterium johnsoniae strain GSE09 shows biocontrol activity against Phytophthora capsici in pepper
[J].
Rhizo-sphere bacteria and fungi associated with plant growth in soils of three replanted apple orchards
[J].
Plant growth promotion rhizobacteria as biofertilizer
[J].
Arbuscular mycorrhizal fungi biofertilizer improves American ginseng (Panax quinquefolius L.) growth under the continuous cropping regime
[J].
Assaying the potential autotoxins and microbial community associated with Rehmannia glutinosa replant problems based on its “autotoxic circle”
[J].




 甘公网安备 62010202000688号
甘公网安备 62010202000688号