0 引言
沙漠生物结皮具有特殊的抗旱机制,对有限的供水会产生快速反应。它们通常在沙漠生态系统演替中发挥重要作用[1-4]。沙漠生物结皮对沙漠中的关键生态系统功能起重要作用,并在沙漠生态系统中起到了开拓和定植作用,可增强沙丘的抗蚀性[5],影响地表入渗,增加保水性[6-7],促进营养供应,减少肥力损失[8-9],改善土壤结构[10-11],影响维管植物的出苗和存活[12]。沙漠生物结皮自然恢复到稳定演替状态可能需要几十年甚至几千年,尽管荒漠化土地中沙漠生物结皮的自我恢复一直在发生[13],但维管植物的定植通常发生在生物结皮改善表土环境之后,这可能需要很长时间,沙漠生物结皮从扰动中的自然恢复因地而异[14]。因此,沙漠生物结皮的快速人工繁殖对沙漠生态系统的恢复具有重要的现实意义[15-16]。
1 材料与方法
1.1 材料
2019年4月,在中国北方腾格里沙漠东南缘的中国科学院沙坡头沙漠研究试验站(37°32′N,105°02′E)收集了沙漠苔藓结皮。该地区的土壤疏松、贫瘠,由含水量为2%—3%的沙粒组成。苔藓结皮主要由银苔藓(Bryum argenteum)和尖叶对齿藓(Didymodon constrictus)组成[31]。将新鲜苔藓结皮放入密封的塑料袋中带回实验室,立即在25 °C温度和120 μE·m-2·s-1光强和保持湿润的条件下在光培养箱中培养7 d。用稀盐酸和氢氧化钠溶液调节培养基的pH值至7.5。光暗循环为12 h∶12 h。将0.5 mg·L-1 6-苄基氨基嘌呤(2,4-D)和40 g·L-1蔗糖加入培养基中,在30 ℃的培养箱中生长60 d。培养的苔藓结皮经过风干粉碎后用于制备生物固沙材料。
将一定量的氢氧化钠溶解在烧杯中的10 mL蒸馏水中。在氢氧化钠溶液中缓慢加入15 mL丙烯酸,在冰水浴中中和,中和度为80%,然后加入一定量的丙烯酰胺,以丙烯酸和丙烯酰胺的质量比15∶4制备单体溶液。取10 g凹凸棒石粉末,溶解于30 mL蒸馏水中,制备凹凸棒石胶体。此外,交联剂N,N’-亚甲基双丙烯酰胺的用量为0.05%,引发剂过硫酸钾和亚硫酸氢钠(过硫酸钾与亚硫酸氢钠的摩尔比为1∶1)的用量为0.6%,溶解于10 mL蒸馏水中,以制备引发剂交联剂溶液。将水浴温度设置为80 ℃,直到温度达到规定值,向单体溶液中加入凹凸棒石胶体和交联剂溶液,然后进行水浴反应。反应8 h,将复合材料置于烘箱中,并在90 °C下干燥直至完全干燥。将干燥材料粉碎至100目,并以1∶3、1∶2、1∶1、0∶1、2∶1、3∶1的比例与苔藓结皮粉末混合均匀,得到6种生物固沙材料,编号为BSM13、BSM12、BSM11、BSM10、BSM21和BSM31。
1.2 实验
将6种生物固沙材料分别以400 g·m-2的比例均匀地铺在直径为15 cm、沙子厚度为1 cm的培养皿中,放置在光照强度为120 μE·m-2·s-1、明暗周期为12 h∶12 h的人工气候培养箱中。在30 °C温度下培养20 d。在试验过程中,每12 h喷水1次,以补充生物固沙材料和沙子的水分。
选择BSM11材料在不同水分和养分供应条件下进行试验。水分梯度为每1、3、6 d供水1次(模拟湿润、半湿润、半干旱环境)。每个水分梯度设置3个营养梯度,营养液与蒸馏水的体积比为1∶0、1∶1、0∶1。溶液每7 d喷洒1次。叶绿素a每20 d测定1次。培养80 d后,测定生物固沙材料的厚度、pH值和抗压强度。
1.3 叶绿素a与生长性状的测定
用乙醇和碳酸钙在加冰的研钵中研磨2 g新鲜样品,然后在黑暗中用95%(v/v)冷却的乙醇提取,并在4 ℃下保持过夜。离心样品(4 000 r·s-1,10 min),然后在665、649、470 nm处测量过滤提取物的叶绿素a含量。使用游标卡尺测量厚度。使用推拉力计进行抗压强度试验。将待测外壳的裂纹判定为失效,并根据应力峰值计算抗压强度。
2 结果与分析
2.1 生长特性
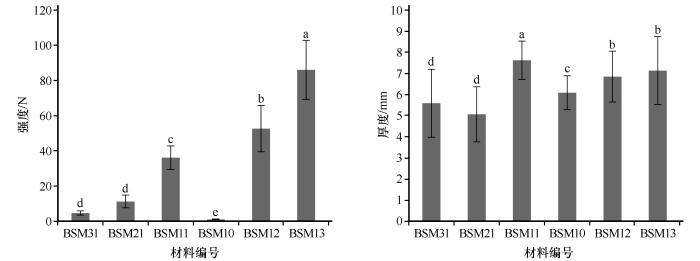
单因素方差分析表明,6种生物型固沙材料的生长厚度和抗压强度表现出显著差异。BSM11的厚度显著高于其他5种材料,BSM31和BSM21之间没有显著差异,BSM10的厚度显著高于BSM31和BSM21,低于BSM12和BSM13(图1)。凹凸棒石可以提高BSMs的抗压强度。
图1
图1
生物固沙材料的强度和厚度
不同小写字母表示差异显著,P<0.05
Fig.1
The strength and thickness of biological sand-fixing materials
2.2 不同培养时间条件下的叶绿素a含量
不同的生物固沙材料、培养时间及其交互作用显著影响叶绿素a含量(表1)。6种生物固沙材料在4个培养时期叶绿素a含量差异显著。20 d时,BSM31、BSM21、BSM10、BSM12和BSM13的叶绿素a含量无显著差异,均显著低于BSM11。40 d时,BSM11、BSM12和BSM13之间以及BSM31、BSM21和BSM10之间的叶绿素a存在不显著差异,前3种材料显著高于后3种材料。60 d时,BSM12和BSM13的叶绿素a含量显著高于BSM31、BSM21和BSM10,低于BSM11,且BSM10、BSM31和BSM21之间不存在显著差异。接种80 d后,BSM10、BSM12、BSM13和BSM21之间没有显著差异,且显著高于BSM31,低于BSM11。与其他生物固沙材料相比,BSM11的叶绿素a含量始终最大。未添加固沙材料的BSM10在所有培养时间的叶绿素a含量均最低(表2)。人工培养生物结皮与固沙材料按1∶1的比例混合使用时,在沙面上表现出更强的存活能力和更有效的光合作用。
表1 6种生物固沙材料和4种培养时间条件下叶绿素a的双因素方差分析
Table 1
| 变异来源 | df | F | P |
|---|---|---|---|
| 生物型固沙材料 | 2 | 129.8 | <0.001 |
| 接种时间 | 2 | 69.40 | <0.001 |
| 交互作用 | 4 | 167.7 | <0.001 |
表2 生物固沙材料应用后叶绿素a含量
Table 2
| 材料编号 | 培养天数/d | F值 | |||
|---|---|---|---|---|---|
| 20 | 40 | 60 | 80 | ||
| BSM31 | 0.180±0.003Ab | 0.184±0.004Ab | 0.196±0.004Ac | 0.127±0.068Bc | 8.24* |
| BSM21 | 0.188±0.001b | 0.194±0.001b | 0.202±0.001c | 0.213±0.001b | 3.45 |
| BSM11 | 0.203±0.002Ba | 0.218±0.001ABa | 0.247±0.006Ba | 0.280±0.008Aa | 8.69* |
| BSM10 | 0.164±0.005Bb | 0.193±0.008Ab | 0.202±0.001Ac | 0.204±0.001Ab | 8.56* |
| BSM12 | 0.195±0.003Cb | 0.214±0.001Ba | 0.218±0.005ABb | 0.228±0.001Ab | 9.78** |
| BSM13 | 0.191±0.002Cb | 0.208±0.001Ba | 0.215±0.001Bb | 0.225±0.001Ab | 9.32* |
| F值 | 6.98* | 10.24** | 9.34** | 8.56* | |
*,P<0.05;**,P<0.01;不同大写字母表示不同培养天数间差异极显著,P<0.05;不同小写字母表示不同固沙材料间差异显著,P<0.05。
BSM31、BSM11、BSM10、BSM12和BSM13处理的叶绿素a含量在所有4个培养时间中均表现出显著差异。BSM21的叶绿素a含量在80 d内没有出现显著变化。对于BSM31,在60 d内没有变化,80 d的叶绿素a含量显著低于前3个培养时间,BSM11出现相反的情况,BSM11的叶绿素a含量在80 d的培养时间达到最大值。对于BSM10,40、60 d和80 d的叶绿素a含量没有表现出显著差异,并且它们显著高于20 d。对于BSM12和BSM13,40 d和60 d的叶绿素a含量显著高于20 d,低于80 d,并且两者都存在显著差异(表2)。叶绿素a含量可以反映人工生物固沙材料的存活和生长能力,在80 d的接种期内,添加更多凹凸棒石可以明显提高生物固沙材料的生存能力。
2.3 不同水分和养分供应条件下的叶绿素a含量
在所有4个培养期,通过BSM11的双因素方差分析,间歇式供水、营养供应及其交互作用显著影响叶绿素a含量(表3)。在20 d的培养期,100%营养条件下,间歇供水对BSM11的叶绿素a含量没有显著影响。50%营养条件下,3 d和1 d的叶绿素a含量没有表现出差异,并且显著高于6 d间歇供水;在3 d间歇供水条件下,50%营养处理显著提高了叶绿素a含量。在40 d培养期,在50%营养条件下,间歇供水对叶绿素a含量没有显著影响,1 d间歇供水条件下的叶绿素a含量始终最高;在3 d间歇供水条件下,营养供应处理对叶绿素a含量没有显著影响。在60 d培养期,3 d间歇供水条件下,3个营养处理的叶绿素a含量显著高于6 d间歇供水,而低于1 d间歇供水处理;50%和100%营养条件下的BSM11叶绿素a含量没有表现出差异,均显著高于蒸馏水处理。在80 d培养期,1 d间歇供水条件下的叶绿素a含量显著高于6 d间歇供水处理,蒸馏水处理3 d和6 d之间不存在显著差异;在50%和100%营养条件下,3 d和1 d间歇供水对BSM11的叶绿素a含量没有显著影响。在持续80 d的接种期内,50%的营养处理和1 d的间歇供水始终促进了生物固沙材料叶绿素a含量的增加(表4)。
表3 不同间歇供水和营养条件下BSM11叶绿素a含量方差的双因素分析
Table 3
| 培养天数/d | 变异来源 | df | F值 | P |
|---|---|---|---|---|
| 20 | 水分 | 2 | 12.85 | <0.001 |
| 营养 | 2 | 29.47 | <0.001 | |
| 水分×营养 | 4 | 16.79 | <0.001 | |
| 40 | 水分 | 2 | 19.86 | <0.001 |
| 营养 | 2 | 45.62 | <0.001 | |
| 水分×营养 | 4 | 17.97 | <0.001 | |
| 60 | 水分 | 2 | 36.25 | <0.001 |
| 营养 | 2 | 17.89 | <0.001 | |
| 水分×营养 | 4 | 123.45 | <0.001 | |
| 80 | 水分 | 2 | 42.35 | <0.001 |
| 营养 | 2 | 51.26 | <0.001 | |
| 水分×营养 | 4 | 15.68 | <0.001 |
表4 不同间歇供水和营养供应条件下BSM11的叶绿素a含量
Table 4
| 培养天数/d | 营养处理 | 间歇供水天数/d | F值 | ||
|---|---|---|---|---|---|
| 6 | 3 | 1 | |||
| 20 | 蒸馏水 | 0.177±0.002Aa | 0.192±0.001Ba | 0.204±0.001Ba | 12.67** |
| 50%营养 | 0.191±0.001Ab | 0.208±0.001Ba | 0.224±0.001Bb | 16.28** | |
| 100%营养 | 0.172±0.005a | 0.187±0.001b | 0.193±0.001a | 2.45 | |
| F值 | 8.35** | 9.82*** | 12.56*** | ||
| 40 | 蒸馏水 | 0.166±0.001A | 0.174±0.001B | 0.181±0.001Bc | 7.35* |
| 50%营养 | 0.171±0.001 | 0.178±0.001 | 0.186±0.001 | 3.14 | |
| 100%营养 | 0.169±0.001A | 0.174±0.001A | 0.183±0.001B | 6.31* | |
| F值 | 2.98 | 2.78 | 3.19 | ||
| 60 | 蒸馏水 | 0.158±0.007Aa | 0.165±0.001Ba | 0.182±0.001Ca | 8.25** |
| 50%营养 | 0.175±0.001Ab | 0.187±0.001Bb | 0.196±0.001Cb | 7.96* | |
| 100%营养 | 0.174±0.001Ab | 0.185±0.002Bb | 0.190±0.001Cb | 9.16** | |
| F值 | 9.24** | 7.36* | 8.25** | ||
| 80 | 蒸馏水 | 0.162±0.007Aa | 0.169±0.001Aa | 0.183±0.001Ba | 8.25** |
| 50%营养 | 0.179±0.001Ab | 0.196±0.001Bb | 0.206±0.001Bb | 7.96* | |
| 100%营养 | 0.180±0.001Ab | 0.195±0.002Bb | 0.198±0.001Bb | 9.16** | |
| F值 | 9.24** | 7.36* | 8.25** | ||
*,P<0.05;**,P<0.01;不同大写字母表示不同间歇供水天数间差异极显著,P<0.05;不同小写字母表示不同营养处理间差异显著,P<0.05。
2.4 不同水分和养分供应条件下的生长性状
根据双因素方差分析结果,间歇供水、营养供应及其交互作用对BSM11的厚度和抗压强度有显著影响(表5)。
表5 水分和营养条件对BSM11发育影响的双因素方差分析
Table 5
| 指标 | 变异来源 | df | F值 | P |
|---|---|---|---|---|
| 厚度 | 水分 | 2 | 30.23 | <0.001 |
| 营养 | 2 | 68.15 | <0.001 | |
| 水分×营养 | 4 | 49.94 | <0.001 | |
| 抗压强度 | 水分 | 2 | 17.24 | <0.001 |
| 营养 | 2 | 2.32 | >0.05 | |
| 水分×营养 | 4 | 11.13 | <0.01 |
单因素方差分析结果表明,蒸馏水处理的6 d和3 d间歇供水处理的厚度没有显著差异,但它们都显著低于1 d间歇供水处理。在50%和100%营养处理下,1 d和3 d间歇供水处理的厚度没有表现出显著差异,并且它们都显著高于6 d间歇供水处理。营养供应显著促进了厚度的增加,50%和100%营养处理之间没有显著差异。1 d间歇式供水和营养处理均能促进BSM11的厚度生长。在蒸馏水和100%营养条件下,间歇供水对BSM11的抗压强度有显著影响。在50%营养处理下,BSM11在1 d和3 d间歇供水条件下的抗压强度差异不显著,均显著高于6 d间歇供水。在6 d间歇供水处理时,各营养供应处理之间不存在显著差异。在3 d和1 d间歇供水的情况下,抗压强度显著差异,50%营养处理最好(表6)。1 d间歇供水处理和50%营养液处理能明显提高BSM11的抗压强度。
表6 不同营养处理和间歇供水条件下BSM11的生长特性
Table 6
| 指标 | 营养处理 | 供水间歇天数/d | F值 | ||
|---|---|---|---|---|---|
| 6 | 3 | 1 | |||
| 厚度/mm | 蒸馏水 | 7.21±1.35A | 7.26±2.05Aa | 8.12±1.26B | 8.25** |
| 50%营养 | 7.75±0.93A | 8.36±1.03Bb | 8.64±1.33B | 7.96* | |
| 100%营养 | 7.41±1.22A | 8.18±0.95Bb | 8.23±2.14B | 9.16** | |
| F值 | 2.24 | 7.36* | 2.25 | ||
| 抗压强度/N | 蒸馏水 | 37.31±6.36A | 37.25±2.05Aa | 38.65±3.25Bab | 1.89 |
| 50%营养 | 37.45±5.36A | 40.23±6.13Bb | 41.26±8.65Ba | 7.96* | |
| 100%营养 | 36.46±1.22A | 36.56±2.15Ba | 35.26±12.14Bb | 2.16 | |
| F值 | 2.24 | 7.36* | 6.32* | ||
*,P<0.05;**,P<0.01;不同大写字母表示不同间歇供水天数间差异极显著,P<0.05;不同小写字母表示不同营养处理间差异显著,P<0.05。
3 结论与讨论
人工生物结皮的质量通常通过叶绿素a含量、厚度和抗压强度进行评估[32]。本研究以叶绿素a为指标,探索生物固沙材料的最佳配比。不同配比的生物型固沙材料在沙表面接种后叶绿素a含量差异显著,人工培养苔藓结皮与固沙材料配比为1∶1时的存活和生长效果最好。根据叶绿素a的含量,凹凸棒石添加显著提高了生物型固沙材料的存活能力和有效的光合作用。
营养处理和间歇供水均能显著影响接种的生物型固沙材料的厚度和强度,营养供应对生物结皮的存活和发育具有积极影响[33]。人工培养或人工固沙实验中,适当增加养分供应能显著改善接种的生物型固沙材料的存活和生长状况。本研究中50%的营养供应处理方式可以明显促进人工沙漠接种的生物型沙漠结皮的厚度和强度,是较为理想的养分供应方式。沙漠地区降水一般为间歇性的,一定的降水强度和频度是影响结皮存活和生长的决定性因素[34-35],本项研究中实施的1 d间歇供水明显改善生物型固沙材料的生长状况,显著提高了接种的生物型固沙材料的厚度和强度,充足和频繁的供水可能是人工接种生物结皮的最关键因素。在生产实践中可以采取适度的人工降水培育措施,以增强人工沙漠结皮的适应能力和存活度,为结皮的自然生长和繁殖创造条件。
参考文献
Production of greenhouse‐grown biocrust mosses and associated cyanobacteria to rehabilitate dryland soil function
[J].
Rapidly restoring biological soil crusts and ecosystem functions in a severely disturbed desert ecosystem
[J].
The role of crust thickness in runoff generation from microbiotic crusts
[J].
Effects of inoculated Microcoleus vaginatus on the structure and function of biological soil crusts of desert
[J].
Responses of microbial activities and soil physical-chemical properties to the successional process of biological soil crusts in the Gurbantunggut Desert,Xingjiang
[J].
Diurnal variations of chlorophyll fluorescence and CO2 exchange of biological soil crusts in different successional stages in the Gurbantunggut Desert of northwestern China
[J].
Inferring the impact of rainfall gradient on biocrusts’ developmental stage and thus on soil physical structures in sand dunes
[J].
Divergence in physiological responses between cyanobacterial and lichen crusts to a gradient of simulated nitrogen deposition
[J].
Soil microbial responses to nitrogen addition in arid ecosystems
[J].
The role of non-rainfall water on physiological activation in desert biological soil crusts
[J].
Response of cyanobacterial soil crusts to moisture and nutrient availability
[J].
Chenet al.Man-made desert algal crusts as affected by environmental factors in Inner Mongolia,China
[J].
Responses of biological soil crusts to rehabilitation strategies
[J].
Effects of drought and salt stresses on man-made cyanobacterial crusts
[J].
What stabilizes biological soil crusts in the Negev Desert?
[J].
Changes in winter snow depth affects photosynthesis and physiological characteristics of biological soil crusts in the Tengger Desert
[J].
苔藓结皮复配凹凸棒基高吸水性固沙材料的生理特性
[J].
Combined application of cyanobacteria with soil fixing chemicals for rapid induction of biological soil crust formation
[J].
Winter snowfall can have a positive effect on photosynthetic carbon fixation and biomass accumulation of biological soil crusts from the Gurbantunggut Desert,China
[J].
Responses of photosynthetic properties and chloroplast ultrastructure of Bryum argenteum from a desert biological soil crust to elevated ultraviolet-bradiation
[J].
Physiological responses of soil crust-forming cyanobacteria to diurnal temperature variation
[J].
Assessment of cultured media for desert moss crust by physiological responses
[J].
Physiological responses of artificial moss biocrusts to dehydration-rehydration process and heat stress on the Loess Plateau,China
[J].
Ecophysiological characterization of early successional biological soil crusts in heavily human-impacted areas
[J].
Effects of sand burial stress on the early developments of cyanobacterial crusts in the field
[J].
Preparation and properties of an organic-inorganic composite superabsorbent based on attapulgite
[J].
Purification of lignocellulose hydrolysate by Org-Attapulgite (Divinyl Benzene-StyreneMethyl acrylate) composite adsorbent
[J].
Development of artificially induced biological soil crusts in fields and their effects on top soil
[J].
Impact of inorganic nitrogen additions on microbes in biological soil crusts
[J].
Biological soil crusts influence carbon release responses following rainfall in a temperate desert,northern China
[J].




 甘公网安备 62010202000688号
甘公网安备 62010202000688号