塔里木河的变迁与罗布泊的演化
1
2009
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
Revealing medicinal constituents of Bistorta vivipara based on non-targeted metabolomics and 16S rDNA gene sequencing technology
1
2024
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
干旱区沙生药用植物生态效益综述
1
2025
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
柽柳根际一株盐单胞菌Bachu 26的分离、鉴定及其盐胁迫下的促生作用研究
1
2024
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
Phytochemical and pharmacological properties of the genus Tamarix:a comprehensive review
1
2024
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
Phytochemical and biological profiles of the genus Phragmites (Family Poaceae):a review
1
2023
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
极端干旱区旱生芦苇叶水势变化及其影响因子研究
1
2012
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
响应面法优化珠芽蓼多糖提取工艺研究
1
2025
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
The microbiome of medicinal plants:diversity and importance for plant growth,quality and health
1
2013
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
Rhizosphere microbiome of arid land medicinal plants and extra cellular enzymes contribute to their abundance
1
2020
... 新疆罗布泊地区位于塔里木盆地的最低洼处,具有极端干旱、高温和强辐照等生境特征,极少生物能够在这种极端的荒漠生境中生存[1].柽柳、芦苇和珠芽蓼作为常见的荒漠植物,不仅在荒漠生态系统中具有重要的生态价值,还在传统医学中发挥着重要作用[2-3].柽柳不仅能通过盐腺排出盐分,改善土壤的微环境[4],其所含的活性成分柽柳黄素还显示出显著的抗肿瘤活性,能够有效诱导肝癌细胞的凋亡[5].芦苇除了具有改善盐渍化土壤的功能外,还因其清热生津、利尿解毒的功效,被广泛用于治疗热病烦渴和肺热咳嗽等症状[6-7].珠芽蓼则在传统藏药和中医中广泛应用,其根茎常用于治疗腹泻和痢疾.珠芽蓼所含的珠芽蓼素具有抗病毒作用[8].这些具有强大抗逆性的药用植物为荒漠生境中的微生物提供了有利的生态位,促进了微生物的定殖和代谢网络的进化,从而增加了荒漠微生物的多样性[9-10]. ...
塔克拉玛干沙漠可培养微生物多样性及抗辐射-抗氧化代谢机制研究
1
2020
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
敦煌莫高窟中细菌多样性的研究
1
2012
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
Beneficial microorganisms:regulating growth and defense for plant welfare
1
2024
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
植物内生细菌介导的植物抗逆性研究进展
1
2020
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
中国沙漠微生物分布及特征
1
2023
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
Renaissance in antibacterial discovery from actinomycetes
1
2008
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
一种最适碳源-氨基酸复配培养基对新疆典型生境土壤微生物分离培养的影响
1
2025
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
沙漠微生物源活性天然产物研究进展
1
2024
... 荒漠微生物作为一类特殊的微生物群体,具有显著的抗逆特性,包括耐受极端干旱环境、抵御高强度紫外线辐射、抑制有害细菌生长以及合成抗生素等多重能力[11-12].这类微生物可通过分泌植物激素促进药用植物的生长发育,同时显著增强宿主植物的抗逆能力[13-14].这种植物与微生物之间的协同作用不仅能促进荒漠药用植物次生代谢产物的积累,还可改善土壤结构与肥力,从而提升荒漠生态系统的稳定性和自我恢复能力[15].此外,由于微生物活性天然产物代谢的特异性和结构多样性,以及其能够穿透真核细胞外膜并阻止细胞大分子和靶酶的合成等特性,其在药物开发领域展现出巨大的潜力[16],荒漠微生物的次级代谢产物中包含多种具有抗肿瘤和抗癌活性的化合物,这些化合物结构类型多样,为癌症治疗提供了新的潜在药物来源[17-18].基于此,本研究聚焦于罗布泊荒漠生态系统,分析该地区可培养细菌的多样性,探索其潜在应用价值,并揭示荒漠药用植物根际的群落结构特征.研究旨在为极端环境中微生物的开发与利用提供科学依据,同时为荒漠生态系统的保护与修复奠定菌株资源. ...
Primer,pipelines,parameters:issues in 16S rRNA gene sequencing
1
2021
... 测序得到的细菌16S rRNA基因序列于网站Ezbiocloud(https://www.ezbiocloud.net/)进行比对分析,比对后序列提交至National Center for Bio⁃technology Information(NCBI).采用16S rRNA 基因相似性阈值98.65%作为潜在新种的鉴定标准[19]. ...
Interactive Tree Of Life (iTOL) v5:an online tool for phylogenetic tree display and annotation
1
2021
... 将提交至国家微生物科学数据中心的16S rRNA基因序列在 EZBioCloud 数据库进行比对(www.ezbiocloud.net);然后用邻接法对序列进行分析,用MEGA11构建系统发育树,并利用在线平台iTOL(https: //itol.embl.de/)[20]进行编辑. ...
Nocardiopsis species:Incidence,ecological roles and adaptations
1
2015
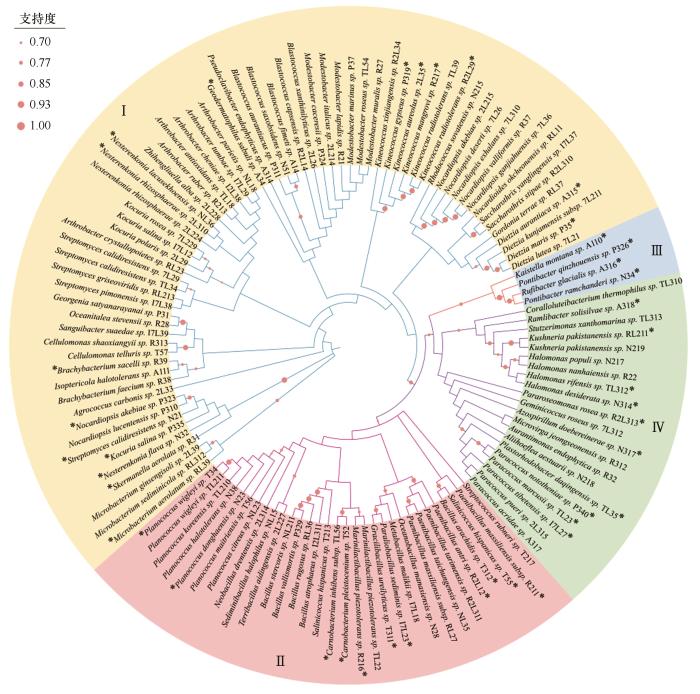
... 序列比对及系统发育树分析表明,在该可培养细菌的系统发育树中,共有41种菌株与其最相似的模式菌株之间的相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种(表2).这些潜在新种来源于27个不同的菌属,其中动球菌属(4株)和涅斯捷连科氏菌属(3株)是潜在新种的优势菌属.这些潜在新种的模式菌株显示出众多应用价值,模式菌株Nocardiopsis akebiae HDS 12T能够产生抗真菌剂帮助宿主植物低于病原菌[21].Microbacterium aerolatum NBRC 103071T能够通过挥发性化合物抑制灰霉病菌(Botrytis cinerea)的生长,减轻灰霉病对植物的危害[22].Streptomyces calidiresistens YIM 78087T的基因组分析显示其具有产生多种次级代谢产物的潜力,在药物开发和工业生物技术中具有重要应用价值[23].这些潜在新种的进一步研究可能有助于填补微生物系统发育树中的空白,还可能为生物技术、医药开发及环境保护等领域带来新的菌株资源. ...
Seed priming by application of Microbacterium spp. strains for control of Botrytis cinerea and growth promotion of lettuce plants
1
2023
... 序列比对及系统发育树分析表明,在该可培养细菌的系统发育树中,共有41种菌株与其最相似的模式菌株之间的相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种(表2).这些潜在新种来源于27个不同的菌属,其中动球菌属(4株)和涅斯捷连科氏菌属(3株)是潜在新种的优势菌属.这些潜在新种的模式菌株显示出众多应用价值,模式菌株Nocardiopsis akebiae HDS 12T能够产生抗真菌剂帮助宿主植物低于病原菌[21].Microbacterium aerolatum NBRC 103071T能够通过挥发性化合物抑制灰霉病菌(Botrytis cinerea)的生长,减轻灰霉病对植物的危害[22].Streptomyces calidiresistens YIM 78087T的基因组分析显示其具有产生多种次级代谢产物的潜力,在药物开发和工业生物技术中具有重要应用价值[23].这些潜在新种的进一步研究可能有助于填补微生物系统发育树中的空白,还可能为生物技术、医药开发及环境保护等领域带来新的菌株资源. ...
Streptomyces calidiresistens sp. nov.,isolated from a hot spring sediment
2
2014
... 序列比对及系统发育树分析表明,在该可培养细菌的系统发育树中,共有41种菌株与其最相似的模式菌株之间的相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种(表2).这些潜在新种来源于27个不同的菌属,其中动球菌属(4株)和涅斯捷连科氏菌属(3株)是潜在新种的优势菌属.这些潜在新种的模式菌株显示出众多应用价值,模式菌株Nocardiopsis akebiae HDS 12T能够产生抗真菌剂帮助宿主植物低于病原菌[21].Microbacterium aerolatum NBRC 103071T能够通过挥发性化合物抑制灰霉病菌(Botrytis cinerea)的生长,减轻灰霉病对植物的危害[22].Streptomyces calidiresistens YIM 78087T的基因组分析显示其具有产生多种次级代谢产物的潜力,在药物开发和工业生物技术中具有重要应用价值[23].这些潜在新种的进一步研究可能有助于填补微生物系统发育树中的空白,还可能为生物技术、医药开发及环境保护等领域带来新的菌株资源. ...
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
罗布泊沙土微生物生态分布特征
1
2009
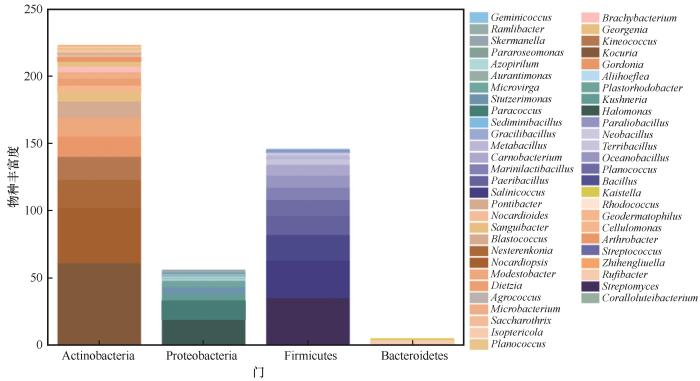
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
罗布泊盐湖可培养放线菌多样性及PKS Ⅱ功能基因筛选
1
2014
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
罗布泊地区沙生植物根际放线菌多样性及生物活性的研究
1
2012
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Increasing aridity reduces soil microbial diversity and abundance in global drylands
1
2015
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Variation of carbohydrate-active enzyme patterns in the gut microbiota of Italian healthy subjects and type 2 diabetes patients
0
2017
Cross-biome metagenomic analyses of soil microbial communities and their functional attributes
0
2012
可培养细菌多样性及抗辐射-抗氧化相关性特征:以库姆塔格沙漠东缘为例
1
2021
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
添加抗生素对新疆特殊生境微生物分离培养的影响
1
2023
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Influence of projection effects on the observed differential rotation rate in the UV corona
1
2013
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Antibiotics,antibiotic resistance genes,and bacterial community composition in fresh water aquaculture environment in China
0
2015
Photosynthetic genes in viral populations with a large genomic size range from Norwegian coastal waters
1
2008
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Exploration of aflatoxin B1 degradation products via Kocuria rosea:structure elucidation and toxicity analysis
1
2024
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
Nocardiopsis species:a potential source of bioactive compounds
1
2016
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
盐水球菌Salinicoccus ventosaetal B2-3-5的代谢产物分析及其抑制酪氨酸酶活性的机制
1
2021
... 罗布泊曾是塔里木河、孔雀河、车尔臣河等河流的终端湖,这一独特的地理位置使其成为了多种生态环境的交汇点,因而为微生物的多样性和分布提供了丰富的生态位[24].罗布泊地区存在丰富的放线菌,且能够产生多种活性次级代谢产物,在生物技术与医药等领域具有广泛的应用前景[25-26].本研究对罗布泊不同生境中的可培养细菌在6种培养基上的菌落数量进行统计分析,结果显示,罗布泊不同生境的可培养细菌归属于放线菌门、拟杆菌门、厚壁菌门和变形菌门,其中放线菌门和厚壁菌门为优势菌门,考克氏菌属、拟诺卡氏菌属和盐水球菌属为优势菌属.放线菌门、厚壁菌门、拟杆菌门和变形菌门是荒漠土壤主要细菌类群[27-30].文凤等[31]从罗布泊地区土样中获得可培养细菌菌属类型与本研究所获得的菌属具有高度一致性.优势菌属考克氏菌属、拟诺卡氏菌属和盐水球菌属是极端环境中常见的可培养细菌优势类群[32-34].从极端环境中分离出的考克氏菌属对多种致病菌具有显著的抗菌活性.玫瑰色考克氏菌(Kocuria rosea)能够有效降解高致癌性的黄曲霉毒素B1,在食品和医疗领域具有重要的应用潜力[35].本研究从沙土环境中分离的菌株P72与模式菌株Kocuria rosea DSM 20447T的16S rRNA基因序列相似度高达99.42%,进一步证实菌株P72为玫瑰色考克氏菌.这一发现不仅丰富了玫瑰色考克氏菌的菌种资源,还为黄曲霉毒素B1的生物降解提供了新的研究材料.拟诺卡氏菌属的菌株大多具有重要的生物学价值,能够产生聚酮类和肽类等具有抗癌作用的生物活性化合物,在药物开发和疾病治疗中具有潜在的应用前景[36].盐水球菌属的菌株同样具有潜在的医学应用价值,能够产生具有抗菌活性的次级代谢产物,对病原菌具有抑制作用[37]. ...
不同时空尺度下土壤微生物群落分布及驱动因素研究进展
1
2024
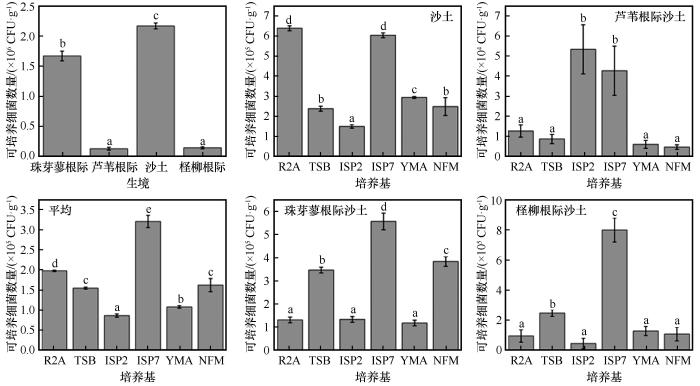
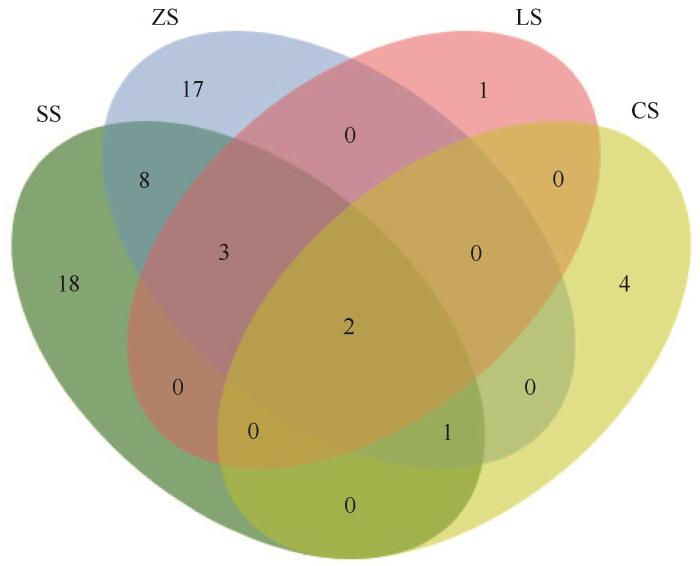
... 在沙土、珠芽蓼根际沙土、柽柳根际沙土和芦苇根际沙土4种生境中,可培养细菌的数量为1.280×105~2.168×106 CFU·g⁻¹,且数量依次为沙土>珠芽蓼根际沙土>柽柳根际沙土>芦苇根际沙土.不同生境中可培养细菌数量及菌属分布存在明显差异:沙土生境的可培养细菌数量及菌属分布最为丰富,珠芽蓼根际沙土的菌属分布和可培养细菌丰度与沙土相似,而柽柳和芦苇根际的细菌丰富度较低.这可能与沙土生境较低的有机质含量和较高的矿物质含量有关,这种环境更有利于耐贫营养细菌的生长[38].相比之下,芦苇与柽柳根际的可培养细菌数量和菌属分布较低,可能与植物根系分泌物的选择性抑制作用有关,这种选择性抑制作用导致植物根际微生物群落的结构趋于单一化,从而减少了可培养细菌的多样性[39-40].珠芽蓼根际的可培养细菌数量和菌属分布与沙土相似,可能是由于珠芽蓼的根系结构相对简单,以须根系为主,没有像柽柳和芦苇那样深且复杂的根系结构,对细菌的选择性富集作用较低导致[41-42]. ...
藏北高寒草原典型植物根际土壤细菌群落结构多样性及根系特征分析
1
2022
... 在沙土、珠芽蓼根际沙土、柽柳根际沙土和芦苇根际沙土4种生境中,可培养细菌的数量为1.280×105~2.168×106 CFU·g⁻¹,且数量依次为沙土>珠芽蓼根际沙土>柽柳根际沙土>芦苇根际沙土.不同生境中可培养细菌数量及菌属分布存在明显差异:沙土生境的可培养细菌数量及菌属分布最为丰富,珠芽蓼根际沙土的菌属分布和可培养细菌丰度与沙土相似,而柽柳和芦苇根际的细菌丰富度较低.这可能与沙土生境较低的有机质含量和较高的矿物质含量有关,这种环境更有利于耐贫营养细菌的生长[38].相比之下,芦苇与柽柳根际的可培养细菌数量和菌属分布较低,可能与植物根系分泌物的选择性抑制作用有关,这种选择性抑制作用导致植物根际微生物群落的结构趋于单一化,从而减少了可培养细菌的多样性[39-40].珠芽蓼根际的可培养细菌数量和菌属分布与沙土相似,可能是由于珠芽蓼的根系结构相对简单,以须根系为主,没有像柽柳和芦苇那样深且复杂的根系结构,对细菌的选择性富集作用较低导致[41-42]. ...
根际微生物群落与促生菌多样性及其筛选策略
1
2012
... 在沙土、珠芽蓼根际沙土、柽柳根际沙土和芦苇根际沙土4种生境中,可培养细菌的数量为1.280×105~2.168×106 CFU·g⁻¹,且数量依次为沙土>珠芽蓼根际沙土>柽柳根际沙土>芦苇根际沙土.不同生境中可培养细菌数量及菌属分布存在明显差异:沙土生境的可培养细菌数量及菌属分布最为丰富,珠芽蓼根际沙土的菌属分布和可培养细菌丰度与沙土相似,而柽柳和芦苇根际的细菌丰富度较低.这可能与沙土生境较低的有机质含量和较高的矿物质含量有关,这种环境更有利于耐贫营养细菌的生长[38].相比之下,芦苇与柽柳根际的可培养细菌数量和菌属分布较低,可能与植物根系分泌物的选择性抑制作用有关,这种选择性抑制作用导致植物根际微生物群落的结构趋于单一化,从而减少了可培养细菌的多样性[39-40].珠芽蓼根际的可培养细菌数量和菌属分布与沙土相似,可能是由于珠芽蓼的根系结构相对简单,以须根系为主,没有像柽柳和芦苇那样深且复杂的根系结构,对细菌的选择性富集作用较低导致[41-42]. ...
根际微生物调控植物根系构型研究进展
1
2016
... 在沙土、珠芽蓼根际沙土、柽柳根际沙土和芦苇根际沙土4种生境中,可培养细菌的数量为1.280×105~2.168×106 CFU·g⁻¹,且数量依次为沙土>珠芽蓼根际沙土>柽柳根际沙土>芦苇根际沙土.不同生境中可培养细菌数量及菌属分布存在明显差异:沙土生境的可培养细菌数量及菌属分布最为丰富,珠芽蓼根际沙土的菌属分布和可培养细菌丰度与沙土相似,而柽柳和芦苇根际的细菌丰富度较低.这可能与沙土生境较低的有机质含量和较高的矿物质含量有关,这种环境更有利于耐贫营养细菌的生长[38].相比之下,芦苇与柽柳根际的可培养细菌数量和菌属分布较低,可能与植物根系分泌物的选择性抑制作用有关,这种选择性抑制作用导致植物根际微生物群落的结构趋于单一化,从而减少了可培养细菌的多样性[39-40].珠芽蓼根际的可培养细菌数量和菌属分布与沙土相似,可能是由于珠芽蓼的根系结构相对简单,以须根系为主,没有像柽柳和芦苇那样深且复杂的根系结构,对细菌的选择性富集作用较低导致[41-42]. ...
植物根际微生物调控根系构型研究
1
2021
... 在沙土、珠芽蓼根际沙土、柽柳根际沙土和芦苇根际沙土4种生境中,可培养细菌的数量为1.280×105~2.168×106 CFU·g⁻¹,且数量依次为沙土>珠芽蓼根际沙土>柽柳根际沙土>芦苇根际沙土.不同生境中可培养细菌数量及菌属分布存在明显差异:沙土生境的可培养细菌数量及菌属分布最为丰富,珠芽蓼根际沙土的菌属分布和可培养细菌丰度与沙土相似,而柽柳和芦苇根际的细菌丰富度较低.这可能与沙土生境较低的有机质含量和较高的矿物质含量有关,这种环境更有利于耐贫营养细菌的生长[38].相比之下,芦苇与柽柳根际的可培养细菌数量和菌属分布较低,可能与植物根系分泌物的选择性抑制作用有关,这种选择性抑制作用导致植物根际微生物群落的结构趋于单一化,从而减少了可培养细菌的多样性[39-40].珠芽蓼根际的可培养细菌数量和菌属分布与沙土相似,可能是由于珠芽蓼的根系结构相对简单,以须根系为主,没有像柽柳和芦苇那样深且复杂的根系结构,对细菌的选择性富集作用较低导致[41-42]. ...
Contributions of beneficial microorganisms in soil remediation and quality improvement of medicinal plants
1
2022
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
植物微生物组生态功能与群落构建过程研究进展
1
2023
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Dynamic root exudate chemistry and microbial substrate preferences drive patterns in rhizosphere microbial community assembly
1
2018
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Plant-microbe interactions before drought influence plant physiological responses to subsequent severe drought
1
2025
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Probiotic model for studying rhizosphere interactions of root exudates and the functional microbiome
1
2024
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Marinilactibacillus piezotolerans sp.nov.,a novel marine lactic acid bacterium isolated from deep sub-seafloor sediment of the Nankai Trough
1
2005
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Streptomyces pimonensis sp.nov.,isolated from the Taklimakan Desert in Xinjiang,China
1
2022
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Two new strains of Streptomyces with metabolic potential for biological control of pear black spot disease
1
2024
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
根际促生菌对植物的生长促进作用及机制研究进展
1
2022
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
滋养节杆菌S17的分离鉴定及其对黄瓜促生能力研究
1
2024
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Choline and osmotic-stress tolerance induced in Arabidopsis by the soil microbe Bacillus subtilis (GB03)
1
2010
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
The Xanthomonas oryzae pv.oryzae type IV pilus alignment subcomplex protein PilN contributes to regulation of bacterial surface‐associated behaviours and T3SS system
1
2020
... 本研究发现珠芽蓼、柽柳和芦苇均与其根际的植物微生物之间存在独特的招募与共生关系,且根际存在的可培养细菌丰度差异显著.植物根际微生物可以通过多种途径促进植物的生长,包括增强植物对养分的吸收、抑制病原菌、激发植物的系统性抗性以及促进次生代谢产物的积累等[43-44].作为反馈,微生物能够促进植物对养分的获取、诱导其系统抗性,从而提升植物对环境的适应能力[45-46].本研究从芦苇根际分离的菌株RL37经鉴定为Gordonia terrae NBRC 100016T的近缘菌株(相似度99.2%),该菌株具有生物固氮和溶解难溶性磷的功能特性,可能通过改善芦苇对N、P营养元素的获取促进其生长[47].另一株分离菌TL29与Marinilactibacillus piezotolerans DSM 16108T(相似度99.29%)具有高度同源性,该菌的耐高压特性提示其可能在宿主应对干旱、盐胁迫等逆境时发挥保护作用[48].此外,从芦苇根际获得的链霉菌属菌株(Streptomyces pimonensis TRM75549T和S. griseoviridis NBRC 12874T)已被证实可通过诱导系统抗性增强植物抗病性[49].其中S. griseoviridis菌株已被成功应用于植物病害的生物防治[50].在珠芽蓼根际微生物组中,Azospirillum doebereinerae GSF71T[51]、Paracoccus acridae SCU-M53T[52]和芽孢杆菌属(Bacillus spp.)菌株同样存在对宿主植物的促生作用[53].柽柳根际分离获得的 Streptomyces calidiresistens YIM 78087T可用于植物病害防治[23],而Kocuria salina Hv14bT则通过溶磷和分泌生长素协同促进植物发育[54].这些发现不仅印证了植物-微生物互作机制的多样性,更为解析不同药用植物根际微生态系统的功能特异性提供了新的视角. ...
Biotransformation of 6∶2/4∶2 fluorotelomer alcohols by Dietzia aurantiaca J3:enzymes and proteomics
1
2024
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Pontibacter ramchanderi sp.nov.,isolated from hexachlorocyclohexane-contaminated pond sediment
1
2013
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Biological treatment of methyl orange dye and textile wastewater using halo-alkaliphilic bacteria under highly alkaline conditions
1
2024
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
耐辐射动球菌耐辐射及相关特性研究进展
1
2016
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Geodermatophilus sabuli sp.nov.,a γ-radiation-resistant actinobacterium isolated from desert limestone
1
2015
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Azospirillum:a free-living nitrogen-fixing bacterium
1
2000
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Potential applications and emerging trends of species of the genus Dietzia:a review
2
2014
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
... [61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...
Comprehensive updates on the biological features and metabolic potential of the versatile extremophilic actinomycete Nocardiopsis dassonvillei
1
2023
... 通过16S rRNA序列比对及系统发育树分析,本研究发现41种可培养细菌菌株与其最相似模式菌株的16S rRNA基因序列相似度低于98.65%,表明这些菌株很可能代表了潜在的微生物新种.尽管16S rRNA基因序列相似性不能直接推断功能特性,但这些潜在新种的模式菌株在多个领域展现出显著的应用潜力,提示其可能具备相似的功能价值.在环境修复领域,模式菌株Dietzia aurantiaca CCUG 35676T能够高效降解全氟烷基和多氟烷基物质,处理顽固的有机污染物[55].Nesterenkonia lacusekhoensis IFAM EL-30T和Pontibacter ramchanderi LP43T分别对偶氮染料和六氯环己烷表现出良好的降解能力[56-57].此外,模式菌株Kineococcus radiotolerans SRS30216T和Geodermatophilus sabuli BMG8133T 具有对高辐射、强碱及重金属的耐受性,是核废料污染场地生物修复的候选菌株[58-59].在农业领域,多株潜在新种的模式菌株展现出固氮、抗病和促生等重要功能.例如,Microbacterium aerolatum NBRC 103071T通过挥发性化合物抑制灰霉病菌的生长,并显著促进生菜幼苗生长(胚根重量增加45%).Azospirillum doebereinerae GSF71T通过固氮作用及植物激素(如吲哚-3-乙酸)的产生,显著增强作物的抗逆性和产量[60].此外,多个潜在新种的模式菌株在生物活性物质开发方面也展现了广阔的前景.例如,Dietzia maris DSM 43672T产生的抗菌代谢物具有靶向牛结核病原体Mycobacterium avium subsp. paratuberculosis(MAP)的能力,且与传统抗生素相比,具有更低的医疗并发症风险[61].Nocardiopsis akebiae HDS12T作为植物内生菌,能够产生抗真菌剂及多种具有抗菌、抗肿瘤和抗氧化特性的生物活性物质,为天然产物的开发提供了新的资源[61].Bacillus arachidis SY8T产生的胞外多糖(EPS)对重金属离子(如Pb(II)、Cu(II))具有高效吸附作用,并且拥有伪塑性和非牛顿流体特性,使其在环境修复和工业材料开发中具有双重应用价值[62]. ...




 甘公网安备 62010202000688号
甘公网安备 62010202000688号