0 引言
在宁夏中北部沙质草地生境,由于长久以来人类活动的干扰,例如过度放牧,再加上干旱的气候条件,草地发生退化、沙化[1]。为了防沙治沙、促进退化植被生态恢复,扎设草方格、建设人工灌丛林来进行生态恢复和生态重建,已被认为是沙漠化治理的有效措施,成功经验已经在非洲、东亚和蒙古国等地区得到广泛采用和推广[2]。随着灌丛的定居、生长发育,风沙活动减弱,土壤环境逐渐得到改善,促进土壤-植被系统向良好方向发展[3]。地面节肢动物是沙地草地生态系统的重要组成部分,对改善土壤质量、加速枯落物分解、加快生物地球化学循环过程具有重要的生态功能,并且对环境条件变化非常敏感[4]。所以,研究沙漠化地段草方格扎设及灌丛林营造对地面节肢动物群落组成、多样性分布特征的影响,对于沙漠化区域人工林建设、生物多样性保护及防沙治沙具有重要意义。
目前,关于灌丛对于节肢动物时空分布影响的研究已有许多报道。Doblas-Miranda等[5]通过对地中海干旱荒漠草原生态系统中不同灌丛生境大型节肢动物组成及其季节变化进行研究,发现灌丛生境能够维持较高的生物多样性、丰富度和生物量。Eldridge等[6]研究了美国新墨西哥州奇瓦瓦荒漠草原不同灌丛群落中长期定居土壤动物群落结构分布特征,认为土壤动物的活动在塑造植被群落和维持或加强荒漠化进程方面具有重要作用。Zhao等[7]发现科尔沁沙地灌丛可以聚集和增加局部大型土壤动物种类、数量和多样性而形成“虫岛”现象。刘继亮等[8]发现灌丛微生境对土壤动物群落分布特征及其结构存在显著影响。灌丛不仅会为土壤动物提供良好的栖息、繁殖场所和食物资源条件,而且灌丛的发育过程及其功能特性还会影响土壤动物在灌丛内外的空间分布,在维持土壤动物群落生物多样性等方面起到重要作用[9]。但是,基于草方格的固沙灌丛林营造对地面节肢动物群落结构的影响规律,尚不清楚。
鉴于此,在宁夏盐池县发生严重沙漠化地段,选择扎设草方格营造的不同灌丛林地为研究对象,以周围流动沙地为对照,通过调查不同生境样地地面节肢动物群落组成、多样性分布及生物量,解析不同固沙灌丛林营造对地面节肢动物群落结构的影响规律,旨在为宁夏荒漠草原人工林建设、生物多样性保护和沙漠化治理提供依据。
1 研究地区与研究方法
1.1 研究地区概况
研究样地位于宁夏盐池县北王圈村(37°52′26.12″N,107°29′44.29″E)。该区域气候属于典型的温带大陆性气候。多年平均气温8.2 ℃,最冷月(1月)气温-7.82 ℃,最热月(7月)气温21.95 ℃。年降水量280 mm,60%以上的降雨在7—9月;年潜在蒸发量2 710 mm。年无霜期165 d。地带性土壤以灰钙土为主,非地带性土壤主要为风沙土。土壤结构松散,肥力较低。
于2011年5月,在研究样地发生严重沙漠化地段,设立固沙试验区,扎设草方格、营造灌丛林。草方格规格:1 m×1 m,然后将试验区划分为4种灌丛林营造区,分别为油蒿(Artemisia ordosica)、花棒(Hedysarum scoparium)、沙拐枣(Calligonum mongolicum)和柠条(Caragana korshinskii)幼苗。每隔1行种植灌丛幼苗1株(幼苗高度30~50 cm),株距1.5 m,行距3 m;幼苗栽植深度30~40 cm(齐地面或略高于地面,避免幼苗受到夏季太阳灼伤)。幼苗栽植在平坦的流动沙地上,微地形坡度5°~10°,地下水深度为>6 m。植被类型为沙地植被,常见植物种类以旱生和中旱生类型为主,主要包括油蒿、花棒、柠条等灌木、亚灌木和苦豆子(Sophora alopecuroides)、中亚白草(Pennisetum centrasiaticum)、猪毛蒿(Artemisia scoparia)等草本植物。
1.2 研究方法
1.2.1 试验设计
于2013年7—8月的植物生长期,即地表节肢动物物种数最高的时期[12],选择草方格扎设并营造有油蒿、花棒、沙拐枣、柠条的4种固沙灌丛林地为研究样地,以周围流动沙地(未扎设草方格且未营造灌丛)为对照样地。5个生境样地均分布在平坦的沙地上,微地形基本相同。每种样地设置5个重复样区,每个重复样区面积1.2~1.7 hm2,间距30 m左右。每个样区布设取样点4个,共100样点。
1.2.2 地面节肢动物调查与标本鉴定
1.2.3 土壤样品采集与测定分析
于2013年7月,在每个调查样点,按照“M”形用100 mL环刀,采集0~10 cm土层新鲜土样5个,混合均匀后用自封袋取500 g土样带回实验室。1/4新鲜土样用于土壤含水量的测定,剩余3/4土样经自然风干后,过2 mm土壤筛除去树根、叶片等杂物,用于土壤颗粒组成及土壤理化性质的测定。同时,在上述采样点附近利用100 mL环刀取原状土样1个,用于土壤容重测定。本部分结果见参考文献[18]。
土壤容重采用环刀法取样和烘干法测定。土壤含水量(%)采用烘干称重法进行测定。土壤颗粒组成(%)采用英国马尔文公司的Mastersizer3000激光粒度仪测定。采用美国农业部分类系统对土壤颗粒进行分级:粗砂粒(250~1 000 μm)、细砂粒(100~250 μm)、极细砂粒(50~100 μm)、黏粉粒(<50 μm)[18]。土壤pH值(水土比悬液为2∶1)和土壤电导率(水土比浸提液为5∶1;μS·m-1)用P4多功能测定仪器测定(Muiti-line P4 Universal Meter,WTW公司,德国)。土壤有机碳(g·kg-1)、土壤全氮(g·kg-1)用元素分析仪(意大利DK6,UDK140分析仪)进行测定。
1.2.4 灌丛幼苗生长特征和地表植被调查
于2013年7月,在每个调查样点附近,布设5 m×5 m样方,调查灌丛个体数(株·m-2)、高度(cm)、冠幅(m2)等指标。同时,布设1 m×1 m样方,调查地表草本植被特征,包括个体数、高度和物种数。本部分结果见参考文献[18]。
1.3 数据处理与分析
将每个样地2次调查所获得的地面节肢动物个体数进行合并计算,以便保证每个灌丛林地的样地代表性和满足统计分析。然后,统计每个样地的地面节肢动物个体数和类群数,在此基础上计算Shannon多样性指数(H)。
式中:
采用SPSS15.0软件进行统计分析。采用单因素方差分析(One-way ANOVA)和Duncan多重比较法比较不同数据组间的差异性。利用字母标记法表示各数据组之间的差异显著性(P<0.05)。应用R软件devtools包和ggvegan包进行多元统计分析运算。首先,采用DCA分析(Detrended correspondence analysis)确定排序轴的最大梯度长度为1.653<3,确定进行RDA分析。然后,利用方差膨胀因子分析,对所有环境因子进行共线性分析,依次删掉最大的变量,也就是删除掉共线性的环境因子,直到所有的变量都小于10;并用step模型检测最低AIC值,自动筛选出最优的环境因子;当“none”位于最顶端时意味着改模型筛选结束,位于none值上方的环境因子即为与节肢动物群落拟合最好的环境因子。最后,利用ANOVA进行显著性检验,得到所筛选的环境因子的整体贡献率以及每个环境因子的单独贡献率,并绘制地面节肢动物群落与解释变量关系的二维排序图。
2 结果与分析
2.1 环境特征
不同类型林地土壤理化性质和植被分布特征存在显著差异性(表1)。土壤粗砂含量表现为油蒿林地最高,流沙和沙拐枣居中,而花棒和柠条最低;土壤细砂表现为沙拐枣最高,花棒和柠条居中,而流沙和油蒿最低;土壤极细砂表现为沙拐枣林地显著低于流沙地和油蒿、花棒和柠条林地;土壤黏粉粒表现为油蒿最高,流沙和柠条居中,而花棒和沙拐枣最低。土壤含水量、电导率、全碳、全氮和C∶N均表现为油蒿最高,而流沙地和花棒、沙拐枣及柠条林地较低。土壤容重表现为沙拐枣和花棒较高,流沙地和柠条居中,而油蒿最低。土壤pH表现为沙拐枣最高,花棒居中,而流沙地、油蒿和柠条林地最低。
表1 不同样地土壤理化性质和植被特征(平均值±标准误)
Table 1
| 土壤植被性状 | 样地 | ||||
|---|---|---|---|---|---|
| 流沙 | 油蒿 | 花棒 | 沙拐枣 | 柠条 | |
| 土壤粗砂粒CS | 3.6±1.2b | 9.0±0.5a | 1.5±0.2c | 2.3±0.3bc | 1.6±0.4c |
| 土壤细砂粒FS | 64.5±6.1bc | 57.9±3.1c | 70.2±4.0b | 85.5±1.6a | 73.4±2.2b |
| 土壤极细砂VFS | 29.1±3.8a | 28.4±3.1a | 27.5±3.8a | 12.0±1.6b | 23.7±2.1a |
| 土壤黏粉粒CpS | 2.8±1.1b | 4.7±0.3a | 0.8±0.2c | 0.2±0.0c | 1.3±0.1bc |
| 土壤含水量SM | 3.7±0.4b | 7.3±0.6a | 2.9±0.4bc | 2.4±0.0c | 3.4±0.2bc |
| 土壤容重BD | 1.4±0.0b | 1.1±0.0c | 1.4±0.0ab | 1.5±0.0a | 1.4±0.0b |
| 土壤电导率EC | 60.4±1.2b | 70.0±2.1a | 57.2±1.1b | 58.8±0.6b | 58.6±0.2b |
| pH | 9.3±0.0b | 9.3±0.0b | 9.4±0.0ab | 9.4±0.0a | 9.4±0.0b |
| 土壤总氮TN | 0.1±0.0b | 0.3±0.0a | 0.1±0.0b | 0.1±0.0b | 0.1±0.0b |
| 土壤有机碳OC | 0.7±0.1b | 4.5±1.3a | 0.4±0.0b | 0.4±0.0b | 0.8±0.4b |
| 土壤C∶N | 6.5±0.3b | 15.6±2.6a | 4.4±0.6b | 5.6±0.7b | 7.2±1.2b |
| 草本植物多度HD | 78.6±9.5b | 255.3±20.3a | 51.2±15.6bc | 14.7±3.4c | 25.2±8.8c |
| 草本植物物种数HR | 4.2±0.6b | 10.0±0.4a | 4.2±0.7b | 1.8±0.3c | 2.0±0.3c |
| 草本植物高度HH | 23.9±2.7a | 10.9±1.3b | 8.9±2.0b | 16.9±0.9ab | 18.5±6.1ab |
| 灌丛高度SH | — | 41.8±2.1c | 48.8±5.6c | 123.0±10.2a | 69.8±3.2b |
| 灌丛冠幅SC | — | 0.4±0.1b | 0.4±0.1b | 2.0±0.3a | 0.3±0.0b |
“—”表示不存在,不同字母表示不同生境差异显著(P<0.05)。
沙拐枣灌丛的高度和冠幅均显著高于其他3种灌丛,而柠条高度显著高于花棒和油蒿。草本植物密度和物种数均表现为油蒿最高,花棒和流沙地次之,而沙拐枣和柠条最低,但植物高度表现为流沙地最高,沙拐枣和柠条林地次之,而油蒿和花棒林地最低。
2.2 地面节肢动物群落组成
调查样地共捕获地面节肢动物853只,隶属于6目13科14个类群(表2)。其中,优势类群为蠼螋科(Labiduridae)、步甲科(Carabidae)和拟步甲科(Tenebrionidae),个体数占总个体数的91.09%;常见类群为蝼蛄科(Gryllotalpidae)、蜣螂科(Geotrupidae)共2个类群,个体数占总个体数的5.86%;其余9类为稀有类群,个体数仅占总个体数的3.05%。
表2 不同样地地面节肢动物群落组成及营养类群的个体数分布(平均值±标准误)
Table 2
| 类群 | 功能群 | 流沙 | 油蒿 | 花棒 | 沙拐枣 | 柠条 | |||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 长奇盲蛛科(Phalangiidae) | Pr | 0.0±0.0 | 0.0±0.0 | 0.2±0.2 | + | 0.0±0.0 | 0.0±0.0 | ||||
| 狼蛛科(Lycosidae) | Pr | 0.0±0.0 | 0.8±0.6 | ++ | 0.2±0.2 | + | 0.0±0.0 | 0.0±0.0 | |||
| 平腹蛛科(Gnaphosidae) | Pr | 0.0±0.0 | 0.0±0.0 | 0.2±0.2 | + | 0.0±0.0 | 0.0±0.0 | ||||
| 光盔蛛科(Liocranidae) | Pr | 0.0±0.0 | 0.2±0.2 | + | 0.0±0.0 | 0.0±0.0 | 0.2±0.2 | + | |||
| 蝼蛄科(Gryllotalpidae) | Ph | 1.8±0.4 | ++ | 1.2±0.2 | ++ | 1.2±0.5 | ++ | 0.6±0.4 | ++ | 2.8±0.7 | ++ |
| 蟋蟀科(Gryllidae) | Ph | 0.0±0.0 | 0.6±0.6 | + | 0.0±0.0 | 0.0±0.0 | 0.0±0.0 | ||||
| 蠼螋科(Labiduridae) | Pr | 10.8±3.1 | +++ | 39.2±11.0 | +++ | 12.4±5.2 | +++ | 6.0±2.0 | +++ | 9.2±3.9 | +++ |
| 步甲科(Carabidae) | Pr | 5.0±1.2 | +++ | 21.8±4.8 | +++ | 8.0±3.2 | +++ | 6.8±2.6 | +++ | 12.0±3.0 | +++ |
| 蜣螂科(Geotrupidae) | Sa | 0.0±0.0 | 2.2±1.0 | ++ | 0.0±0.0 | 0.0±0.0 | 0.2±0.2 | + | |||
| 葬甲科(Silphidae) | Sa | 0.0±0.0 | 0.4±0.2 | + | 0.0±0.0 | 0.0±0.0 | 0.0±0.0 | ||||
| 阎甲科(Histeridae) | Sa | 0.0±0.0 | 0.0±0.0 | 0.4±0.4 | ++ | 0.4±0.4 | ++ | 0.0±0.0 | |||
| 拟步甲科(Tenebrionidae) | Ph | 4.0±1.3 | +++ | 0.6±0.2 | + | 11.4±3.9 | +++ | 4.2±1.5 | +++ | 4.0±2.4 | +++ |
| 步甲科幼虫(Larval Carabidae) | Pr | 0.2±0.2 | + | 0.2±0.2 | + | 0.0±0.0 | 0.0±0.0 | 0.0±0.0 | |||
| 蚁科(Formicidae) | Om | 0.0±0.0 | 1.2±0.8 | ++ | 0.0±0.0 | 0.0±0.0 | 0.0±0.0 |
捕食性=Pr,植食性=Ph,腐食性=Sa,杂食性=Om. +表示稀有类群,++表示常见类群,+++表示优势类群。
从表2可以看出,流动沙地共有5个类群,优势类群、常见类群和稀有类群的类群数分别为3、1、1,其个体数占本样地总个体数的90.8%、8.3%、0.9%。相对于流动沙地,油蒿林地的节肢动物优势类群、常见类群和稀有类群的类群数分别为2、4、5,其个体数所占比例分别为89.2%、7.9%、2.9%。花棒林地的节肢动物优势类群、常见类群和稀有类群的类群数分别为3、2、3,其个体数所占比例分别为93.5%、4.7%、1.8%。沙拐枣林地的节肢动物优势类群、常见类群和稀有类群的类群数分别为3、2、0,其个体数所占比例分别为94.4%、5.6%、0。柠条林地的节肢动物优势类群、常见类群和稀有类群的类群数分别为3、2、1,其个体数所占比例分别为88.7%、9.9%、1.4%。
流动沙地优势类群包括蠼螋科、步甲科和拟步甲科3个类群,而花棒、沙拐枣和柠条林地的节肢动物优势类群亦包括蠼螋科、步甲科和拟步甲科3个相同类群,但油蒿林地优势类群则仅包括蠼螋科和步甲科2个类群。
2.3 地面节肢动物群落多样性
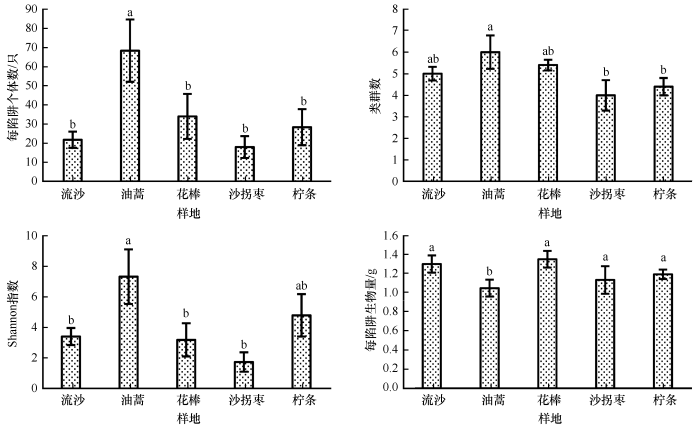
地面节肢动物个体数表现为油蒿灌丛林地显著高于流动沙地(P<0.05,图1),而花棒、沙拐枣及柠条林地和流动沙地间无显著差异性。类群数表现为油蒿林地最高,沙拐枣和柠条林地最低,而流动沙地和花棒林地居中。Shannon指数表现为油蒿林地最高,流动沙地、花棒和沙拐枣林地最低,而柠条林地居中。生物量表现为油蒿林地显著低于流动沙地、花棒和沙拐枣及柠条林地(P<0.05)。
图1
图1
不同样地地面节肢动物群落多样性分布
不同小写字母表示不同生境的差异性,P<0.05
Fig.1
The diversity distribution of ground-active arthropod communities in different sampling sites
2.4 地面节肢动物功能群结构
依据食性划分,调查获得的地面节肢动物共包括捕食性、植食性、腐食性和杂食性4个营养类群,分别有7、3、3、1个类群,其个体数分别占总个体数的78.19%、18.99%、2.11%、0.71%(表2)。由于杂食性动物只有1个类群,即蚁科(Formicidae),而且仅在油蒿林地捕获到个体,每陷阱个体数1.2±0.8只,故本文仅比较其余3个营养类群的分布情况。
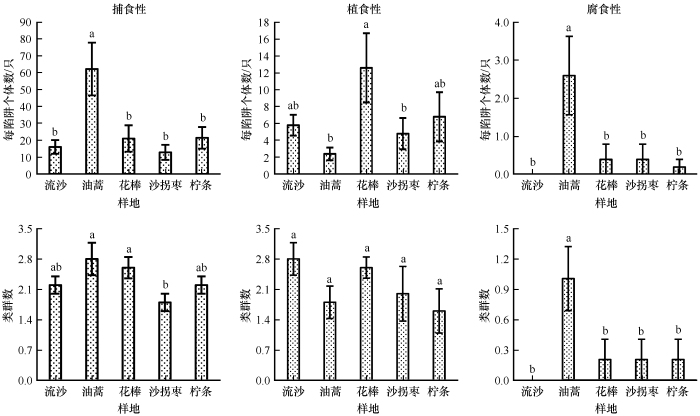
捕食性动物和腐食性的个体数分布规律相似,均表现为油蒿灌丛林地显著高于流动沙地(P<0.05,图2),而花棒、沙拐枣及柠条林地和流动沙地间无显著差异性。植食性动物的个体数表现为花棒最高,油蒿和沙拐枣林地最低,而流动沙地和柠条林地居中(P<0.05)。
图2
图2
不同样地地面节肢动物功能群个体数与类群数分布
不同小写字母表示不同生境的差异性(P<0.05)
Fig.2
The abundance and richness of trophic groups of ground-active arthropods in different sampling sites
捕食性动物的类群数表现为油蒿和花棒林地最高,沙拐枣林地最低,而流动沙地和柠条林地居中(P<0.05)。腐食性动物的类群数表现为油蒿灌丛林地显著高于流动沙地(P<0.05),而花棒、沙拐枣及柠条林地和流动沙地间无显著差异性。植食性动物的类群数则表现为不同样地间无显著差异性(P>0.05)。
2.5 地面节肢动物群落分布与环境因子的关系
图3
图3
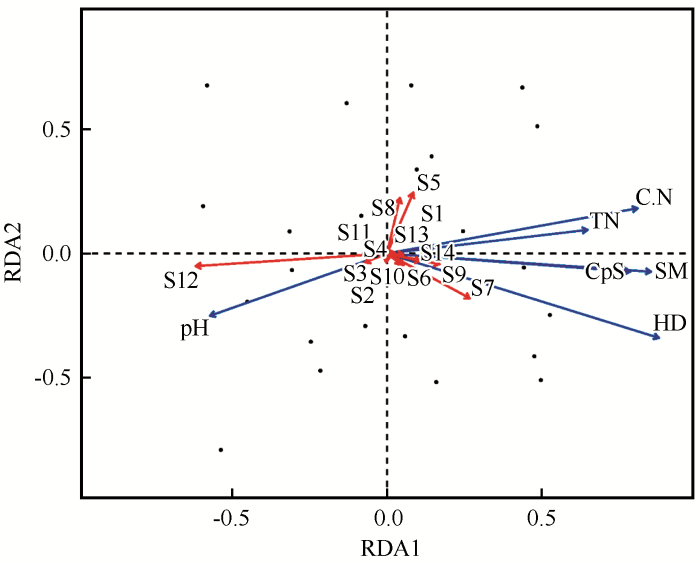
地面节肢动物群落分布与环境因子关系的RDA二维排序图
圆形,样地;长奇盲蛛科,S1;狼蛛科,S2;平腹蛛科,S3;光盔蛛科,S4;蝼蛄科,S5;蟋蟀科,S6;蠼螋科,S7;步甲科,S8;蜣螂科,S9;葬甲科,S10;阎甲科,S11;拟步甲科,S12;步甲科幼虫,S13;蚁科,S14;草本植物多度,HD;土壤含水量,SM;土壤C∶N,C.N;土壤黏粉粒,CpS;土壤全氮,TN;土壤pH,pH.
Fig.3
B iplot of RDA showing the relationship between ground-active arthropods and environmental factors
表3 环境因子对地面节肢动物群落分布的相对贡献率
Table 3
| 环境因子 | Df | 方差 | F | Pr(>F) |
|---|---|---|---|---|
| 草本植物多度HD | 1 | 0.032 | 6.906 | 0.001** |
| 土壤含水量SM | 1 | 0.005 | 1.136 | 0.310 |
| 土壤C∶N | 1 | 0.005 | 1.125 | 0.331 |
| 土壤黏粉粒CpS | 1 | 0.004 | 0.857 | 0.468 |
| 土壤全氮TN | 1 | 0.006 | 1.321 | 0.262 |
| pH | 1 | 0.005 | 1.203 | 0.307 |
| 残差 | 18 | 0.085 |
3 讨论与结论
在草地发生严重沙漠化地段开展扎设草方格营造灌木林,已被认为是防沙治沙、退化草地生态系统结构与功能恢复的有效手段,得到了大面积推广应用。随着流动沙地逐渐固定,土壤理化性质及地表植被在共同促进了退化草地生态系统演变的同时,亦对生存于其中的地面节肢动物群落组成与分布产生了深刻影响[19]。本调查结果显示,蠼螋科和步甲科及拟步甲科是优势类群(表2)。步甲科、拟步甲科反映了一种对荒漠、半荒漠生境的生理生态学适应性[20],这与刘继亮等[8]在黑河中游、Sackmann等[21]在南美荒漠草原的研究结果相似。捕食性动物包括步甲科和蠼螋科个体数分布较多,原因可能在于降雨集中的8—9月处于植物生长季且植食性动物个体数增加,为这些捕食性动物提供了重要的食物来源[22],故其种类和数量均会增多,反映了它们对沙地环境的较强适应性。
本研究中,相对于流动沙地,花棒、沙拐枣和柠条林地的地面节肢动物优势类群均为蠼螋科、步甲科和拟步甲科,但油蒿林地的优势类群则为蠼螋科、步甲科,这与油蒿林地土壤含水量较高密切相关。王晶等[22]在塔克拉玛干沙漠中的研究发现,步甲科个体喜土壤湿度较高的绿洲区生境。刘继亮等[23]在黑河流域荒漠区发现蠼螋科偏好在沙质、湿润的柽柳人工林生境中生活。这说明油蒿林人工固沙植被恢复,可能提高了土壤水分的有效性而改变蠼螋科及步甲科甲虫个体的分布。相对于流动沙地,油蒿、花棒和柠条林地节肢动物稀有类群的类群数变化较大,优势类群和稀有类群的优势度增加,而常见类群的优势度下降,但沙拐枣林地无稀有类群出现。一方面说明不同灌丛林营造固沙措施对地面节肢动物群落组成产生不同的影响,即油蒿、花棒和柠条林地均有助于增加地面节肢动物的稀有类群数,而沙拐枣林地对地面节肢动物类群组成的影响有限。同时,也说明了油蒿、花棒和柠条林地对地面节肢动物类群组成恢复产生了积极作用[24]。
群落多样性有两方面的含义:其一是群落所含物种数的多寡,即物种丰富度,群落所含的物种数越多,多样性就越高;其二是群落各个种的相对多度,即群落的均匀性,均匀性越高的群落,其异质性就越大,说明多样性也越高[25-26]。本调查结果显示,油蒿林地地面节肢动物个体数、类群数和Shannon指数均高于其他林地,但花棒、沙拐枣和柠条林地地面节肢动物多样性与流动沙地间无显著差异性。刘新民等[27]在腾格里沙漠研究中发现,在以干旱为特征的植物群落中的优势植物种(油蒿)是大部分动物类群的主要食物资源和生活场所。这说明沙化地段营造油蒿灌木林有助于地面节肢动物多样性的快速提升,即油蒿林地地面节肢动物丰富度越高,其多样性越高[28]。而柠条、沙拐枣和花棒均属于灌木,生长较油蒿慢,故其对土壤和植被的短期影响也小,结果导致这3种生境地表节肢动物群落与流动沙地接近,这和前期关于柠条和花棒能够提供地面节肢动物多样性的影响结果[29]不同,因此未来需要进一步长期跟踪监测。
功能群划分反映了不同节肢动物类群间营养级联关系[32]。本研究结果表明,捕食性和植食性动物类群构成了地面节肢动物群落的主要功能群,特别是捕食性动物占据绝对优势地位,反映了研究区域地面节肢动物区系以捕食性动物分布为其主要特征[12]。油蒿林地捕食性和腐食性动物类群的个体数和类群数均较多,说明油蒿林地有助于延伸食物链长度,不仅包括食物链上端的捕食性类群,而且还包括营腐食性物质为主的腐食性动物类群,有利于物质循环过程和能量流动[30]。同时,油蒿林地植食性动物类群个体数较低,反映了一种下行控制效应[33]。上行/下行理论(Bottom-up/top-down theory)综合了资源营养物质的上行作用和捕食者捕食作用的下行影响。虽然两者间在概念的表述上存在差异,实际上并无本质区别,都是以捕食者为调控的主要因子的理论,可看作为同一理论体系[33]。本调查结果说明油蒿林营造能够在提高节肢动物多样性的同时,亦能够调控植食性害虫的发生。但是,花棒林地植食性类群个体数则较高,反映了豆科灌丛植物对植食性节肢动物的吸引力[23]。原因在于花棒作为豆科植物,能够为更多的植食性节肢动物个体提供适口性较好的食物资源[7]。
不同灌木林由于其自身的生理生态学特性而导致产生不同的生态效应。罗雅曦等[18]研究发现不同灌丛林营造后其自身的生长状况变化较大,并且对土壤环境和地表植被亦产生不同的影响。土壤环境为地面节肢动物提供了栖息地,地表植被分布为地面节肢动物提供了食物来源,而且土壤动物类群数量的多少、组成的变化和密度的大小通常决定于土壤环境条件的优劣和食物资源的有效性[34]。所以,不同灌丛林营造后通过土壤环境和地表植被对地面节肢动物群落组成和多样性分布产生了深刻影响。本研究结果表明,草本植物多度是影响地面节肢动物多度的主要因素(表3),这与张安宁等[35]和杨贵军等[12]的研究结果相似,但与李岳诚等[36]的研究结果并不一致。杨贵军等[12]在宁夏盐池荒漠草原发现植被密度和植被盖度是影响整个步甲群落活动密度的决定因素。但李岳诚等[36]在宁夏灵武白芨滩荒漠生境中发现植被物种密度对地表甲虫的影响相对较弱。这说明不同的生态系统类型中,由于不同土壤动物类群对环境变化的响应模式不同,从而决定了地表节肢动物群落个体数分布特征,从而影响到节肢动物的营养功能群组成及其食物网结构的动态变化[23]。
蠼螋科和步甲科及拟步甲科是调查样地地面节肢动物群落的优势类群。油蒿、柠条和花棒林营造均可以增加地面节肢动物的稀有类群的类群数,而沙拐枣林营造效果有限。油蒿林地能够显著增加地面节肢动物的多样性。从功能群的角度来看,油蒿、沙拐枣、花棒和柠条等植物短期恢复对地表节肢动物营养结构的影响不同,油蒿林营造可以显著增加捕食性和腐食性动物类群的个体数和类群数,而花棒更有利于植食性动物类群的个体数增加。
参考文献
Sand barriers of straw checkerboards for habitat restoration in extremely arid desert regions
[J].
Long-term ecosystem effects of sand-binding vegetation in the Tengger desert,Northern China
[J].
Soil macroinvertebrate fauna of a Mediterranean arid system:composition and temporal changes in the assemblage
[J].
Impacts of shrub encroachment on ecosystem structure and functioning: towards a global synthesis
[J].
The “bug island” effect of shrubs and its formation mechanism in Horqin Sand Land,Inner Mongolia
[J].
Different microhabitats affect soil macroinvertebrate assemblages in a Mediterranean arid ecosystem
[J].
Influence of shrubs on soil characteristics and their function in Sahelian agro-ecosystems in semi-arid Niger
[J].
Shrubs and species identity effects on the distribution and diversity of ground-dwelling arthropods in a Gobi desert
[J].
Facilitative effects of shrubs in shifting sand on soil macro-faunal community in Horqin Sand Land of Inner Mongolia,Northern China
[J].
Carabid Beetles: Ecology and Evolution
[M].
Temporal and spatial patterns of tenebrionid beetle diversity in NW Patagonia,Argentina
[J].
Shrub cover expressed as an ‘arthropod island’ in xeric environments
[J].
Trophic interactions in an arid ecosystem: from decomposers to top-predators
[J].




 甘公网安备 62010202000688号
甘公网安备 62010202000688号